Гипоксия в родах. Помощь остеопата
Гипоксически-ишемическое поражение центральной нервной системы перинатального генеза – это очень частый диагноз, с которым обращаются родители со своими детьми. 75-85% заболеваний нервной системы у детей своими истоками уходят в ранние сроки внутриутробного развития или проблемы в родах. Внутриматочная гипоксия и гипоксия в родах обуславливают нарушения маточно-плацентарного кровообращения, что может сопровождаться недостатком кислорода у плода. Гипоксические нарушения у детей часто связаны с функциональным дисбалансом, ограничением кровотока и движения ликвора. Остеопатия нормализует движения в теле и способствует питанию мозга, исправлению негативных послествий перенесенной гипоксии.
Гипоксия и асфиксия, происходящие в родах и в период новорожденности, не проходят бесследно и могут оказать негативное воздействие на развивающийся мозг. Исходом может стать значительная потеря нейронов, дистрофические изменения нервных клеток в коре головного мозга и в подкорковых структурах и желудочках головного мозга.
В клинической картине могут быть такие симптомы:
При дефиците кислорода нарушается ауторегуляция мозгового кровообращения, изменяется проницаемость нейронов, нарушается обмен веществ в нервных клетках, скапливаются вредные аминокислоты и свободные радикалы. В результате токсических действий этих веществ наступает гибель нейронов, возникает запрограммированная смерть нервных клеток. С учетом прогрессирования деформации нейронов, клинические симптомы могут проявиться позже, через несколько лет. Это говорит о том, что дети после перенесенной гипоксии должны наблюдаться неврологом и остеопатом.
Диагностика гипоксии
Дети с диагнозом перинатальное постгипоксическое поражение ЦНС наблюдаются неврологом в течение 2 лет. По истечении этого срока диагноз снимается, либо меняется на более сложный (ДЦП, гидроцефалия и тд).
Методы диагностики постгипоксического состояния:
- УЗИ головного мозга показывает анатомию нервной системы
- электроэнцефалограмма (ЭЭГ) характеризует функцию нейронов
- допплерография сосудов головного мозга характеризует функции сосудов мозга, с какой скоростью и симметричностью они работают и насколько качественно доставляют кислород мозгу.

- МРТ крайне редко делается детям в первые 2 года, так как требуется наркоз для проведения этого исследования.
На УЗИ головного мозга определяются следующие постгипоксические изменения:
- Кисты (появляются уже после 10-14 дня после гипоксии).
- Деформация извилин и борозд головного мозга.
- Перивентрикулярная лейкомаляция – некроз клеток мозга вокруг желудочков мозга, является в плане прогноза крайне неприятным симптомом, часто заканчивается гидроцефалией и ДЦП.
- Увеличение размеров желудочков мозга, межполушарной щели и других ликворосодержащих пространств.
Периодичность проведения исследований у детей, перенесших гипоксию, 1 раз в 3 месяца до года и 1 раз в 6 мес. на втором году жизни.
Оценка по шкале Апгар не единственный критерий перенесенной гипоксии. Например, у плода, в ответ на недостаток кислорода, открывается сфинктер прямой кишки и меконий выходит в околоплодные воды, из-за чего они становятся зелеными. О кислородном голодании может свидетельствовать также состояние плаценты (преждевременное старение, аномалия развития сосудов, и т.д.). Иногда такие дети рождаются с высокой оценкой по шкале Апгар, но гипоксия все-таки имела место.
О кислородном голодании может свидетельствовать также состояние плаценты (преждевременное старение, аномалия развития сосудов, и т.д.). Иногда такие дети рождаются с высокой оценкой по шкале Апгар, но гипоксия все-таки имела место.
Мозг детей в первые 2 года жизни очень пластичный и с удовольствием принимает все методы лечения, быстро откликается и выдаёт прекрасные результаты. В последнее время остеопатическое лечение занимает заслуженное место в программе лечения детей, перенесших гипоксию.
Последствия гипоксии
Ранее мы рассматривали причины и диагностику постгипоксических состояний и договорились о том, что дети, родившиеся с оценкой 7 баллов по Апгар и ниже, рассматриваются как перенесшие гипоксию. К этой группе также относятся дети, имевшие обвитие пуповиной, недоношенные дети и т.д.
Крайне важно регулярно проводить осмотры таких детей в динамике в определенные возрастные периоды: 1 мес., 3 мес., 6 мес., 9 мес., 1 год. Целью осмотра и наблюдения является профилактика и уменьшение хронических заболеваний и снижение степени отдаленных последствий. Около 83% детей, перенесших гипоксию, имеют поражения ЦНС в различных проявлениях и сочетаниях.
Около 83% детей, перенесших гипоксию, имеют поражения ЦНС в различных проявлениях и сочетаниях.
В течении заболевания выделяют 3 периода:
- острый период до 1 мес.
- восстановительный период с 2 мес. до 2 лет
- исход заболевания — после 2 лет.
Самые частые симптомы поражения ЦНС в остром и восстановительном периоде. Иногда эти симптомы проявляются в сочетании друг с другом:
- Синдром повышенной нервно-рефлекторной возбудимости.
- Ребенок очень беспокойный, негативный к осмотру, отмечаются нарушения сна, нарушения мышечного тонуса и т.д.
- Гипертензионно-гидроцефальный синдром.
- Из-за увеличения количества жидкости в пространствах головного мозга повышается внутричерепное давление. Характеризуется быстрым темпом прироста окружности головы, большим родничком, беспокойным поведением, частыми срыгиваниями.
- Вегето-висцеральный синдром.

- Нарушение функций ЖКТ, частые срыгивания, частый стул или запоры, вздутие живота. Нарушение регуляции тонуса сосудов, которое проявляется как неравномерность окраски кожи (мраморность). Нарушение ритма дыхания и сердечных сокращений.
- Синдром угнетения ЦНС.
- Снижение двигательной активности, снижение тонуса мышц, ослабление рефлексов сосания и глотания.
- Пирамидный синдром.
Выражается гипертнусом икроножных мышц, тугоподвижностью в голеностопных суставах, хождением на цыпочках, задержкой темпов речевого развития, а также двигательного.
При наличии данных симптомов не стоит дожидаться планового осмотра, лучше сразу обратиться к неврологу и остеопату для ранней диагностики и лечения.
Лечение гипоксии
Постгипоксическое поражение ЦНС требует этапного лечения после проведения реанимационных мероприятий (если они были необходимы) начинается восстановительный период, применяется:
- ЛФК
- массаж
- физиотерапевтическое лечение
- медикаментозная терапия (ноотропные препараты, сосудистые препараты, витамины)
- гидрокинезотерапия (плавание)
- все активнее применяются такие методы, как бобат-терапия, войта-терапия, которые особенно полезны для детей с нарушением мышечного тонуса
- остеопатия.

Остеопатическое лечение гипоксии в родах
Остеопатическое лечение по праву занимает одно из ведущих мест в реабилитации детей, перенесших гипоксию. Балансировка костей черепа позволяет снять напряжение с твердой мозговой оболочки и с полушарий головного мозга, тем самым обеспечивая максимально полноценное функционирование ЦНС.
Остеопатические методики позволяют осуществить дренаж венозных синусов, в результате чего налаживается резорбция ликвора и нормализуется внутричерепное давление. Освобождение шейного отдела позвоночника, устранение кривошеи способствует адекватному кровоснабжению головного мозга.
Раннее проведение остеопатического лечения на первом году жизни позволяет детям не только не отставать в развитии от своих сверстников, но иногда даже развиваться с опережением. Очень важно проводить это лечение с первых месяцев жизни, так как это поможет избавиться от отдаленных клинических патологических симптомов. Сеансы остеопатии детям проводятся начиная с первого месяца жизни.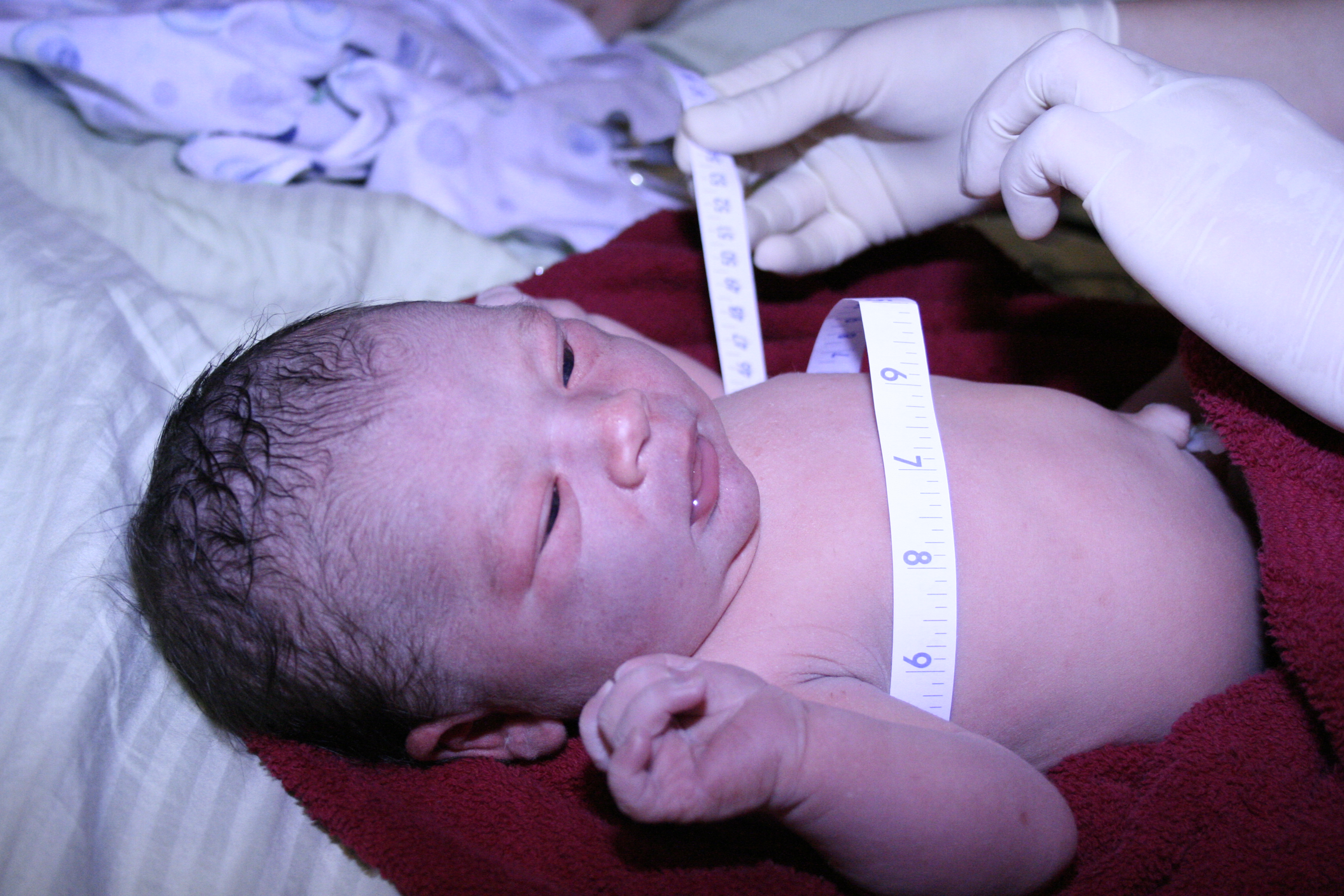 Остеопатическое лечение, создавая оптимальное функционирование ЦНС останавливает процесс постгипоксических изменений в нейронах, тем самым как-бы перепрограммирует мозг на полноценное развитие.
Остеопатическое лечение, создавая оптимальное функционирование ЦНС останавливает процесс постгипоксических изменений в нейронах, тем самым как-бы перепрограммирует мозг на полноценное развитие.
Не нужно бояться гипоксии, нужно предпринять весь комплекс мер для реабилитации после неё. Тем более, что современная медицина даёт нам множество инструментов для этого.
Преимущества лечения последствий гипоксии родов в нашем медицинском центре Неонатус Санус
Наша клиника остеопатии и неврологии на Васильевском острове «Неонатус Санус » — здоровье с рождения, имеет большой практический опыт профилактики и лечении новорожденных детей, младенцев и детей грудничкового возраста.
Мы умеем и любим работать с маленькими детьми!
В нашей клинике работают опытные врачи-остеопаты, неврологи. Каждому малышу уделяется много внимания, чтобы понять ребенка, точно оценить его состояние, дать рекомендации родителям и при необходимости провести эффективное остеопатическое лечение.
В нашем центре вы можете получить лучшее обследование, лечение и рекомендации от ведущих специалистов Санкт-Петербурга.
Клинический пример лечения последствий гипоксии в нашем остеопатическом центре
Отзыв наших пациентов о лечении гипоксии
Катюша родилась от первой беременности на сроке 40 недель. Состояние после рождения было тяжелым за счёт асфиксии. Оценка по шкале Апгар 1/4 балла. Через 3 часа в связи с дыхательной недостаточностью и судорогами была переведена на реанимационное отделение. Проводилась искусственная вентиляция легких, гипотермия мозга.
Результатом тяжелой гипоксии мозга явился диагноз: Детский Церебральный Паралич, правосторонний спастический гемипарез. В возрасте 1 года 6 месяцев она впервые появилась в нашем центре. Основной жалобой была задержка двигательного развития, ходьба самостоятельная появилась только в 1год и 4 месяца. При ходьбе испытывала большие проблемы в связи с высоким гипертонусом мышц по всей правой стороне, отмечалось косоглазие и беспокойное поведение.
После проведённого лечения у девочки практически нормализовался мышечный тонус, походка максимально приблизилась к физиологической, у девочки прекрасное речевое развитие, она с удовольствием ходит в детский сад и общается со сверстниками.
Благодарим родителей за предоставленный видеоматериал.
Видеоотзыв смотрите по сслыке
Гипоксия лечение. Симптомы и лечение у ребенка лечение гипоксии
Строго говоря, гипоксия — это не диагноз. Так называется состояние, когда организм по тем или иным причинам не получает необходимого для полноценного функционирования количества кислорода. Она может возникать не только у новорожденных, но и у людей взрослого возраста, различны лишь причины, из-за которых возникает кислородное голодание. Следствием гипоксии является нарушение работы жизненно важных органов вплоть до необратимых изменений. Наиболее опасно это состояние для центральной нервной системы. Именно головной мозг получает 20 % всего поступающего в кровь кислорода, поэтому гипоксия может обусловить возникновение неврологических заболеваний.
При возникновении гипоксии симптомы и лечение (если оно вообще требуется) зависят от степени кислородного голодания.
Симптомы гипоксии у детей определяются еще при родах. Сразу после появления ребенка медперсонал оценивает его состояние по шкале Апгар. При этом по 10-балльной системе оценивается состояние кожных покровов, рефлекторной возбудимости и тонуса мышц.
Различают три степени гипоксии:
- 8–10 баллов — означает отличное состояние новорожденного;
- 7–6 баллов — гипоксия первой степени, считающаяся легкой формой;
- 5–4 баллов — гипоксия второй степени, классифицируемая как средняя форма;
- 3–0 баллов — третья степень гипоксии, тяжелая форма.
Кислородное голодание легкой степени обычно не сказывается на дальнейшем развитии ребенка, ее симптомы проходят очень быстро. Такая гипоксия лечения не требует.
Гипоксия 2-й степени при должном уходе и лечении редко становится причиной нарушений нормальной работы организма. В первые месяцы лечения возможны нарушения нормального режима сна, тревожность, тремор подбородка.
В первые месяцы лечения возможны нарушения нормального режима сна, тревожность, тремор подбородка.
Тяжелая степень гипоксии может вызвать серьезные последствия в организме ребенка — нередки судороги, задержки в развитии, различные нарушения работы головного мозга.
Если лечение ребенка, перенесшего гипоксию, не начать вовремя, то возможны различные физические и умственные нарушения в развитии. Часто последствиями гипоксии являются гипертонус, задержки психоречевого развития, аутизм, ДЦП, в редких случаях вероятен летальный исход.
Избежать всего этого можно, если еще в раннем возрасте начать лечение последствий гипоксии. Вот почему при выявлении диагноза «гипоксия» у ребенка лечение нужно начинать как можно раньше. В медицинском центре «Клиника Мельниковой Е.А» проводится полная диагностика раннего выявления нарушений работы головного мозга, после которой высококвалифицированные специалисты дадут все рекомендации для родственников и индивидуально подберут курс лечения. Головной мозг ребёнка очень чувствителен к гипоксическому повреждению, но в то же время очень пластичен, т. е. от природы наделен восстановительными и компенсаторными функциями. Поэтому лечение гипоксии и ее последствий по методикам, разработанным главврачом нашей Клиники — врачом-невропатологом высшей категории Мельниковой Е.А. — дает наилучшие положительные результаты при своевременном обращении.
Головной мозг ребёнка очень чувствителен к гипоксическому повреждению, но в то же время очень пластичен, т. е. от природы наделен восстановительными и компенсаторными функциями. Поэтому лечение гипоксии и ее последствий по методикам, разработанным главврачом нашей Клиники — врачом-невропатологом высшей категории Мельниковой Е.А. — дает наилучшие положительные результаты при своевременном обращении.
Гипоксия плода
Из-за недостаточного снабжения кислородом плода, которое называют гипоксией, в его организме происходят неблагоприятные изменения. В общем количестве родов она составляет 10,5%.
Последствиями кислородной недостаточности являются нарушение функций организма, изменение обменных процессов. Для плода последствия от кислородной недостаточности могут быть различны. Они зависят от срока беременности. Гипоксия плода на ранних сроках беременности приводит к появлению отклонений и задерживает развитие эмбриона. В более поздние сроки беременности кислородное голодание вызывает задержку роста плода, поражение центральной нервной системы, понижение адаптационных возможностей новорожденного.
Гипоксия плода не относится к самостоятельным заболеваниям. Она является следствием разнообразных патологических процессов в организме матери, плода и в плаценте. Гипоксия плода по длительности течения делится на острую и хроническую. Острая развивается внезапно, чаще встречается при родах, чем во время беременности. Хроническая развивается на протяжении продолжительного времени, т.е. во время беременности.
Развитию гипоксии плода способствуют множество факторов. Это могут быть заболевания матери, такие как: сердечно-сосудистые и легочные заболевания, анемия, интоксикация и другие. Это могут быть и нарушения плодово-плацентарного кровотока: гестозы, перенашивание плода, риск преждевременных родов, патологии плаценты и пуповины, различные аномалии родовой деятельности. Это могут быть и заболевания самого плода: гемолитическая болезнь или анемия, инфицирование или врожденные пороки развития, длительное сдавливание головки во время родов.
Многочисленны и механизмы развития гипоксии плода./nurse-and-premature-baby-103771589-59a82bc6845b3400118e3614.jpg) Это могут быть: нарушения поставки кислорода к матке, снижение обменных функций плаценты, дефицит гемоглобина в организме матери, сердечно-сосудистые заболевания, нарушение кровотока.
Это могут быть: нарушения поставки кислорода к матке, снижение обменных функций плаценты, дефицит гемоглобина в организме матери, сердечно-сосудистые заболевания, нарушение кровотока.
Выраженные компенсаторные способности плода обусловлены увеличением частоты сердечных сокращений до 150-160 уд/мин, высокой кислородной емкостью крови, уникальным строением гемоглобина, особенностью кровообращения и обменом веществ плода.
Процессы обмена веществ у плода изменяются с уменьшением насыщения крови кислородом. При этом все органы и системы плода за счет компенсаторных возможностей вначале работают с повышенной активностью, однако постепенно наступает их угнетение. Усугубление течения заболевания может привести к непоправимым изменениям.
На здоровье будущего ребенка незначительная гипоксия плода обычно не влияет. Однако гипоксия плода в тяжелой форме может сопровождаться ишемией и некрозами в разных органах, последствия в этом случае могут быть необратимы.
Гипоксию плода можно попытаться выявить самостоятельно, наблюдая за изменением двигательной активности плода. Начальная стадия характеризуется неугомонностью плода, повышением частоты и силы шевелений.
Начальная стадия характеризуется неугомонностью плода, повышением частоты и силы шевелений.
Длительная или прогрессирующая гипоксия плода приводит к ослаблению его движений.
Поводом для срочной консультации у врача служит уменьшение шевелений плода до 3 раз в течение часа. Это свидетельствует о страданиях плода. В этом случае проведут дополнительное обследование околоплодных вод, кардиотокографию, допплерометрию и т.д.
Самыми точными и информативными методами оценки состояния плода являются кардиотокография и допплерометрия. Основным симптомом гипоксии плода при родах является нарушение его сердечной деятельности. Поэтому кардиомониторное наблюдение за состоянием плода широко используется в родах. Если околоплодные воды окрашиваются меконием, т.е. становятся зелеными, значит у плода может быть гипоксия. Однако, этот признак существенен только, если плод лежит головой вперед.
Если у беременной хроническая внутриутробная гипоксия плода, то ей важен покой, т.к. улучшению кровоснабжения матки весьма способствует постельный режим. Хроническую гипоксию плода лечат комплексно, уделяя при этом особое внимание основному заболеванию, которое к ней привело. Проводят терапию, призванную улучшить снабжение плода кислородом и нормализацию обменных процессов. Если эффект от комплексной терапии отсутствует, и срок беременности превышает 28 недель, то принимают решение об экстренных родах путем кесарева сечения.
улучшению кровоснабжения матки весьма способствует постельный режим. Хроническую гипоксию плода лечат комплексно, уделяя при этом особое внимание основному заболеванию, которое к ней привело. Проводят терапию, призванную улучшить снабжение плода кислородом и нормализацию обменных процессов. Если эффект от комплексной терапии отсутствует, и срок беременности превышает 28 недель, то принимают решение об экстренных родах путем кесарева сечения.
За течением беременности важно наблюдать очень тщательно, чтобы предотвратить, либо вовремя диагностировать и вылечить гипоксию плода.
Современным, доступным и эффективным средством в борьбе с гипоксией является профилактическая кислородотерапия, в том числе при помощи кислородного коктейля.
Научные материалы и исследования:
Энтеральная оксигенотерапия в акушерской и гинекологической практике, Кубицкая Ю.В., Ипатова М.В. (Русский Медицинский Журнал)
Эффективность энтеральной оксигенации в комплексной профилактике и лечении ранней плацентарной недостаточности при невынашивании, Радзинский В./female-doctor-examining-newborn-baby-in-incubator-73773081-81cd1d224f294f028abeb7eec2af2442.jpg) Е., Ордиянц И.М., Абдурахманова О.Г. (Русский Медицинский Журнал)
Е., Ордиянц И.М., Абдурахманова О.Г. (Русский Медицинский Журнал)
Оксигенотерапия в ранние сроки беременности, Радзинский В.Е., Ордиянц И.М., Абдурахманова О.Г. (Русский Медицинский Журнал)
Позвоните нам сейчас по телефону , и мы подберем Вам оптимальную комбинацию оборудования для производства кислородного коктейля!
Дополнительный кислород для беременных и для всех людей является по сути лекарством.
Перед применением обязательно проконсультируйтесь с врачом!
Причины острой интранатальной и постнатальной гипоксии у новорожденных | Перепелица
1. Володин Н.Н.
2. Островская О.В., Ивахнишина Н.М., Наговицына Е.Б., Власова М.А., Морозова О.И.Инфекционные факторы при перинатальной смертности.Бюл. Федерального центра сердца, крови и эндокринологии им. ВА. Алмазова.2010; 6: 49—50.
Алмазова.2010; 6: 49—50.
3. Перепелица С.А., Голубев А.М., Мороз В.В.Дыхательная недостаточность у недоношенных детей, рожденных от многоплодной беременности.Общая реаниматология.2010; 6 (6): 18—24.
4. Перепелица С.А., Голубев А.М., Мороз В.В., Шмакова М.А.Прена-тальный морфогенез легких и предпосылки для развития РДС у недоношенных новорожденных.Общая реаниматология.2010; 6 (6): 53—58.
5. Ньюэлл М.Л., Мак-Интайр Дж.(ред.). Врожденные и перинатальные инфекции: Предупреждение, диагностика и лечение. СПб.; 2004.
6. Дубова Е.А., Павлов К.А., Боровкова Е.И., Байрамова М.А., Макаров И.О., Щеголев А.И.Фактор роста эндотелия сосудов и его рецепторы в плаценте беременных с ожирением. Бюл. эксперим. биологии и медицины.2011; 151 (2): 218—223.
Бюл. эксперим. биологии и медицины.2011; 151 (2): 218—223.
7. Дубова ЕА., Павлов КА., Есаян Р.М., Дегтярева Е.И., Шестакова М.В., Щеголев А.И., СухихГ.Т.Фактор роста эндотелия сосудов и его рецепторы в плаценте беременных, страдающих сахарным диабетом 1-го типа.Бюл. эксперим. биологии и медицины.2011; 152 (9): 337—341.
8. Перепелица С.А., Голубев А.М., Мороз В.В.Респираторный дистресс-синдром новорожденных: ранняя диагностика, профилактика и лечение.Общая реаниматология.2012; 8 (4): 95—102.
9. Краснопольский В.И., Логутова Л.С., Туманова ВА., Савельев С.В., Титченко Л.И., Баринова И.В., Пырсикова Ж.Ю., Барыкина О.П., Аксенова А.А., Артюков И.А., Виноградов А.В., Барабанов В.М., Дубинина В.Ю., Романова С.А.Клиническая, ультразвуковая и морфологическая характеристики хронической плацентарной недостаточности. Акушерство и гинекология.2006; 1: 13—16.
Акушерство и гинекология.2006; 1: 13—16.
10. Афанасьева Н.Ф., Стрижаков А.Н.Исходы беременности и родов при фетоплацентарной недостаточности различной степени тяжести.Вопросы гинекологии, акушерства и перинатологии.2004; 2 (3): 1—13.
11. Барашнев Ю.И.Перинатальная неврология. М.: Триада-Х; 2001: 325.
12. Перепелица С.А., Голубев А.М., Мороз В.В., Алексеева С.В., Мельниченко ВА.Воспалительные изменения в плаценте и бактериальная инфекция у недоношенных новорожденных с дыхательной недостаточностью.Общая реаниматология.2012; 8 (3): 18—24.
13. Зубков В.В., Михайлова О.И., Тютюник В.Л.Особенности раннего неонатального периода и первого года жизни детей, родившихся у матерей с плацентарной недостаточностью инфекционного генеза. Вопросы практич. педиатрии.2010; 5 (2): 13—17.
Вопросы практич. педиатрии.2010; 5 (2): 13—17.
14. Перепелица С.А., Голубев А.М., Мороз В.В.Особенности рентгенологических изменений в легких у недоношенных новорожденных с дыхательной недостаточностью.Общая реаниматология.2011; 7 (1): 25—30.
Гипоксия плода. Симптомы, признаки, последствия | Капсула Жизни
Гипоксия плода – опасный патологический процесс, характеризуемый пониженным снабжением кислородом плода.
Гипоксия возникает по причине нетипичных процессов, проходящих в женском организме. Время формирования, протекания и интенсивности проявления симптомов напрямую влияют на развитие и общее состояние здоровья ребёнка. Лечение гипоксии необходимо проводить как можно раньше, чтобы болезнь не нанесла непоправимых последствий.
Гипоксия может диагностироваться на любом сроке беременности. Чем раньше возникнет внутриутробная гипоксия плода, тем более серьёзно она повлияет на развитие ребёнка (как умственное, так и физическое). Также она может нанести ущерб ЦНС, но это в случае несвоевременного или неправильного лечения. Медицинская статистика показывает, что в 10-15% из всех беременностей наблюдается кислородная недостаточность. Лечение в этом случае в первую очередь направлено на приведение в норму потока крови к матке и плаценте, но при острой гипоксии плода рекомендуется вызывать роды искусственным способом, а не применять какие-либо способы лечения.
Также она может нанести ущерб ЦНС, но это в случае несвоевременного или неправильного лечения. Медицинская статистика показывает, что в 10-15% из всех беременностей наблюдается кислородная недостаточность. Лечение в этом случае в первую очередь направлено на приведение в норму потока крови к матке и плаценте, но при острой гипоксии плода рекомендуется вызывать роды искусственным способом, а не применять какие-либо способы лечения.
Внутриутробная гипоксия плода
Причины внутриутробной гипоксии плода – разные патологии, протекающие в материнском организме, а также неблагоприятные факторы внешней среды. Гипоксия может возникнуть из-за заболеваний:
- гипертония
- сахарный диабет
- порок сердца
- преэклампсия и эклампсия
- хронический бронхит или бронхиальная астма
- различные заболевания почек
Внутриутробные причины возникновения гипоксии:
- повреждение целостности матки
- продолжительное передавливание головы, шеи ребёнка при родах
- усложнение прохода малыша по родовому каналу, чаще всего возникает по причине больших объёмов или неправильной позы малыша
- увеличение объёма околоплодной жидкости
- беременность двумя, тремя и более плодами
- внутриутробное заражение ребёнка
- перегораживание плацентой родового прохода из матки
- обматывание пуповины вокруг шеи ребёнка
- нарушение потока крови в плаценте
Кроме этого, весомыми причинами внутриутробной гипоксии плода могут быть внешние факторы:
- плохая экология и высокая загрязнённость воздуха в том месте, где проживает будущая мать
- приём большого количества лекарственных препаратов
- отравление химическими веществами
- злоупотребление женщиной в период беременности спиртными напитками, никотином или наркотиками
Степени гипоксии плода
По скорости протекания гипоксия делится на:
- кратковременная, т.
 е. возникает быстро и неожиданно
е. возникает быстро и неожиданно - средней тяжести – выражается непосредственно во время родов
- острая – признаки болезни наблюдаются за несколько дней до предстоящих родов
- хроническая гипоксия плода – появляется она при сильном токсикозе, несовместимости групп крови или резус-факторов матери и ребёнка, внутриутробных инфекциях плода.
По времени возникновения гипоксия делится:
- образовавшееся на первых месяцах беременности
- во второй половине из отведённого срока
- во время родов
- после родов возникает очень редко.
Симптомы гипоксии плода
Определяется гипоксия довольно сложно, так как она может проявиться внезапно. Но диагностировать гипоксию очень важно именно на ранних этапах, потому что это позволит быстро начать лечение и избежать последствий.
Главным симптомом гипоксии плода является замедленное сердцебиение, но это невозможно заметить в домашних условиях. Первым признаком для консультирования у врача становится изменение интенсивности толчков плода. Каждая женщина ощущает шевеление, но если ребёнок даёт о себе знать менее трёх раз в день, следует немедленно обращаться к специалистам, потому как это свидетельствует о хронической внутриутробной гипоксии плода.
Каждая женщина ощущает шевеление, но если ребёнок даёт о себе знать менее трёх раз в день, следует немедленно обращаться к специалистам, потому как это свидетельствует о хронической внутриутробной гипоксии плода.
Острая форма, возникающая внезапно, характеризуется совершенно противоположными признаками — ребёнок чересчур активен, сильно толкается.
Признаки гипоксии плода в первые три месяца беременности очень сложно определить, поэтому для женщины и плода будет лучше проходить обследования у врача еженедельно.
Последствия гипоксии плода
При игнорировании симптомов или при позднем обращением к врачу, гипоксия серьезно угрожает здоровью и развитию плода.
Осложнениями хронической гипоксии плода могут стать:
- нарушения развития и формирования внутренних органов, костей и головного мозга плода
- внутриклеточные отёки
- внутренние кровоизлияния
- задержка в развитии плода
Для новорождённого ребёнка последствия не менее тяжкие:
- изменения в строении и структуре некоторых внутренних органов; кровоизлияния
- неспособность самостоятельно выполнять функции, характерные для первых дней после рождения
- болезни неврологического характера
- задержка в умственном развитии
- психические отклонения
- ДЦП и аутизм
Острая и хроническая гипоксия плода может привести к смерти плода в утробе или летальному исходу ребёнка на протяжении первой недели жизни.
Как определить гипоксию плода
Определить гипоксию плода начиная с пятого месяца беременности не составит труда. Намного сложнее это сделать на первых 3-х месяцах, но чем раньше будет поставлен диагноз, тем выше вероятность избежать последствий заболевания.
Диагностика гипоксии плода состоит из:
- при помощи специальных гинекологических диагностических методик проводится оценка прозрачности, цвета и количества околоплодных вод
- допплерометрии, которая позволяет отследить скорость потока крови в пуповине и плаценте
- УЗИ
- КТГ
- прослушивания через стетоскоп частоты сердцебиения
- наблюдения за интенсивностью движений плода
Лечение гипоксии плода
При первых же проявлениях симптомов гипоксии плода беременную женщину незамедлительно госпитализируют. Первое, на что направлено лечение, это стабилизация подачи кислорода к плоду и понижение тонуса матки. Для этого пациентке назначают строгий постельный режим и приём лекарственных препаратов, которые улучшат проходимость кислорода и метаболизм. Часто также назначают оксигенотерапию и гипербарическую оксигенацию (барокамеру), что позволяет повысить оксигенацию крови не только в организме матери, но и плода.
Часто также назначают оксигенотерапию и гипербарическую оксигенацию (барокамеру), что позволяет повысить оксигенацию крови не только в организме матери, но и плода.
Когда наблюдаются первые улучшения состояния плода, женщина может выполнять гимнастику, различные дыхательные упражнения, посещать аквагимнастику. Если никакие меры для нормализации подачи кислорода к плоду не дали должного эффекта или симптомы гипоксии плода сохраняются более двадцати восьми недель беременности, лучше всего немедленно провести кесарево сечение. В случае острой гипоксии для новорождённого ребёнка необходима помощь реаниматолога.
Профилактика гипоксии плода
Профилактику гипоксии плода должна выполнять женщина, которая решила стать матерью, а именно:
- правильно выбрать способ рождения ребёнка. При кесаревом сечении меньше шансов на возникновение гипоксии плода, чем при естественных родах
- своевременное лечение болезней, которые сопутствуют беременности
- избегать сильных физических нагрузок, только дыхательная гимнастика
- отдыхать достаточное количество времени
- рационализировать питание, путём употребления большого количества витаминов и кальция
- вести здоровый образ жизни, отказаться от алкоголя, никотина и наркотиков
- регулярно наблюдаться в женской консультации
- вовремя становиться на учёт к акушеру-гинекологу
- планировать беременность и тщательно к ней подготавливаться, путём обследования у врачей, лечения хронических, инфекционных или гинекологических заболеваний
Существует много исследований, связанных с лечением гипоксии плода. Одно из них — применение баротерапии в лечении гипоксии плода
Одно из них — применение баротерапии в лечении гипоксии плода
Другие статьи о баротерапии, оксигенотерапии и барокамерах можно почитать у нас на канале Яндекс.Дзен. Подписывайтесь → канал «Капсула Жизни» в Дзене
Наш сайт: Capsule-life.ru
Гипоксия победима!
Сегодня половине (!) беременных женщин, проживающих в крупных городах, гинекологи ставят диагноз «гипоксия плода». Мы привыкли считать знакомое нестрашным. Если же потратить 15 минут на самообразование в проблеме гипоксии, можно понять:
1) насколько она опасна,
2) ее можно избежать,
3) недуги ребенка, рожденного даже в тяжелой степени гипоксии, поддаются лечению (все зависит от усердия родителей).
О проблеме гипоксии нас консультирует заведующая отделением патологи беременности роддома N7 Ирина Хабировна Байрамова.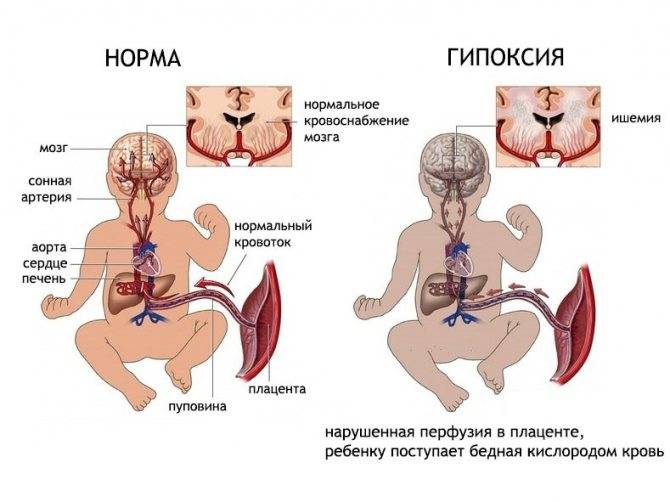
КАК ВОЗНИКАЕТ ГИПОКСИЯ
Кислород и питательные вещества поступают к плоду через маточно-плацентарный кровоток. При нарушениях этого кровотока плод получает недостаточно питательных веществ и кислорода. Этот недостаток и называют гипоксией.
Гипоксия всегда является результатом плацентарной недостаточности (нарушения функций и раннего старения плаценты). Поэтому поиск причин гипоксии — в причинах плацентарной недостаточности. А их немало:
— Инфекционные заболевания, особенно протекающие в острой форме или обостряющиеся во время беременности. В особой группе риска — женщины, не пролечившие до беременности инфекции, передающиеся половым путем.
— Различные хронические заболевания, имеющиеся у беременной (заболевания сердечнососудистой системы, почек, печени, легких).
— Гормональные нарушения в организме беременной.
— Иммунологические проблемы (например, иммунологический конфликт между мужем и женой).
Совет по избежанию этой группы причин — обследоваться до наступления беременности и пролечивать все свои недуги, дабы они не повлияли на здоровье будущего малыша. Если не получилось до беременности — в крайнем случае, в первом триместре.
Если не получилось до беременности — в крайнем случае, в первом триместре.
— Угроза прерывания беременности тоже вызывает гипоксию плода. Это состояние характеризуется повышенным сокращением мускулатуры матки, а это опять же вызывает ухудшение кровотока в матке и плаценте, и, следовательно, ограничивает приток кислорода и питательных веществ к плоду.
— Гестоз — коварное осложнение беременности, при котором питательные вещества и кислород проходят «мимо» плода (выводятся выделительной системой женщины). Даже легкий гестоз, незаметный внешне в виде отеков на теле беременной, вызывает отек плаценты и, как следствие, гипоксию.
Совет: если врач ставит вам эти диагнозы и предлагает лечение в стационаре, не отказывайтесь. Не думайте, что отеки или тянущие боли внизу живота — это только «ваши» проблемы. Данные патологии неизбежно ведут к гипоксии плода, которая обуславливает различные пороки его развития.
Для большей убедительности напомним, что в хронической форме гипоксия оказывает влияние на отклонения в развитии плода, в острой — на его жизнь. Острая форма гипоксии, вызванная повышенным тонусом матки, проявляется как одномоментный спазм сосудов маточно-плацентарного кровотока, при котором доступ кислорода к плоду прерывается. Без немедленного оказания медицинской помощи жизнь плода — под угрозой. Острая форма гипоксии, вызванная тяжелым гестозом, проявляется как отслойка плаценты. Жизнь плода в этом случае может спасти только экстренное родоразрешение.
Острая форма гипоксии, вызванная повышенным тонусом матки, проявляется как одномоментный спазм сосудов маточно-плацентарного кровотока, при котором доступ кислорода к плоду прерывается. Без немедленного оказания медицинской помощи жизнь плода — под угрозой. Острая форма гипоксии, вызванная тяжелым гестозом, проявляется как отслойка плаценты. Жизнь плода в этом случае может спасти только экстренное родоразрешение.
КАК ПРОЯВЛЯЕТСЯ ГИПОКСИЯ У НОВОРОЖДЕННОГО
В первые минуты жизни новорожденного неонатолог оценивает пять показателей его жизнеспособности по шкале Апгар:
— сердцебиение
— дыхание
— цвет кожных покров
— мышечный тонус
— наличие врожденных рефлексов
За каждый показатель в норме выставляется по 2 балла. Малыш на 9-10 баллов полностью здоров: розовенький, мышцы в тонусе (ручки и ножки прижаты к животу, голова — к груди, есть сосательный и хватательный рефлексы, крик громкий, свидетельствующий о нормальном запуске дыхательной системы, сердечный тон четкий, ясный. 8 баллов свидетельствуют о легкой степени гипоксии плода (может наблюдаться, например, незначительная синюшность кожных покровов). О средней степени гипоксии говорят, когда ребенок рождается с немного синенькими ладошками, стопами, лицом, ручки в суставах слегка разогнуты, сосет ребенок слабо, кричит тоже слабо (6 баллов). Тяжелая степень гипоксии проявляется в том, что кожные покровы новорожденного бледные, ручки и ножки разогнуты, крика нет, сосание очень слабое или отсутствует, сердцебиение есть (4 балла).
8 баллов свидетельствуют о легкой степени гипоксии плода (может наблюдаться, например, незначительная синюшность кожных покровов). О средней степени гипоксии говорят, когда ребенок рождается с немного синенькими ладошками, стопами, лицом, ручки в суставах слегка разогнуты, сосет ребенок слабо, кричит тоже слабо (6 баллов). Тяжелая степень гипоксии проявляется в том, что кожные покровы новорожденного бледные, ручки и ножки разогнуты, крика нет, сосание очень слабое или отсутствует, сердцебиение есть (4 балла).
ПОСЛЕДСТВИЯ ГИПОКСИИ
Доказано, что наиболее кислородозависимыми являются нервные клетки, поэтому от гипоксии в первую очередь страдает центральная нервная система плода. В зависимости от степени гипоксии неврологические нарушения новорожденного варьируются от функциональных (обратимых) расстройств (например, пониженный мышечный тонус, снижение активности врожденных рефлексов) до тяжелых нарушений психического развития.
Интересно, что организм плода обладает огромными компенсаторными способностями, поэтому при первых проявлениях гипоксии организм малыша начинает работать в усиленном режиме, перераспределяя кислородные потоки на критически важные для жизни органы и системы: головной мозг, сердце, надпочечники. Естественно, при этом лишаются своей «нормальной порции» кислорода и питательных веществ другие органы — легкие, почки, желудочно-кишечный тракт, кожные покровы. В них-то и могут возникнуть патологии развития в том случае, если организм плода справляется с задачей спасения от пороков развития центральной нервной системы. Однако возможности компенсаторных механизмов имеют предел, и при длительной гипоксии эта защита ослабевает.
У детей, рожденных со средней или тяжелой степенью гипоксии в период новорожденности могут наблюдаться следующие нарушения развития:
- гипотрофия (недостаточный вес),
- снижение мышечного тонуса и угнетение физиологических рефлексов (сосание, хватание),
- синдром дыхательных расстройств,
- аномалии развития — дисплазия тазобедренных суставов, кривошея, пороки сердца и др.
В будущем при отсутствии лечения дети, страдавшие гипоксией в период внутриутробного развития, могут испытывать:
- задержку развития физических и психических навыков,
- повышенное внутричерепное давление,
- частые ОРВИ и кишечные расстройства,
- синдром повышенной возбудимости.
Любые состояния гипоксии, зафиксированные на момент рождения ребенка, лечатся, — успокаивает Ирина Хабировна Байрамова. — Если в течение первого года жизни ребенка приложить все усилия для устранения последствий гипоксии, то к году ваш малыш не будет отличаться по психофизическому развитию от своих сверстников. Последствия легкой гипоксии хорошо лечатся с помощью массажей и упражнений для отдельных групп мышц. Особенно хорошо помогают упражнения в воде, поскольку они стимулируют психо-эмоциональную сферу ребенка, восстанавливая тем самым поврежденные в результате гипоксии участки мозга. Более тяжелые формы гипоксии лечат непосредственно в роддоме медикаментозными методами. Даже при хороших результатах лечения родителям важно знать, что теперь их ребенку особенно важно регулярно наблюдаться у врачей разных специальностей, главными из которых являются педиатр и невролог. Они будут осуществлять контроль за развитием психического здоровья малыша, исключать поздние проявления пороков развития нервной системы.
ПОБЕДИТЬ ГИПОКСИЮ
Еще лучше лечить гипоксию плода внутриутробно, чтобы предотвратить знакомство с описанными выше неприятными диагнозами у своего малыша.
Диагноз «гипоксия плода» ваш акушер-гинеколог может поставить не ранее 28 недели беременности. Он делает это, выслушивая сердцебиение плода стетоскопом. Нормальное сердцебиение плода — 120-160 ударов в минуту. Если оно больше или меньше, можно подозревать о наличии гипоксии. Чтобы сказать наверняка, врачу необходимы результаты исследований КТГ (электрокардиограмма плода), УЗИ (смотрится степень зрелости плаценты и качество околоплодных вод). В некоторых случаях для уточнения диагноза необходимо проведение допплеровского исследования (показывает наличие или отсутствие проблем сосудистого кровотока в матке и плаценте).
Если данные исследования указывают на наличие средней и тяжелой степени гипоксии, беременной обязательно нужно ложиться в стационар. Без уточняющих вопросов «А обязательно ли это?». » Я рекомендую полежать в стационаре и пройти курс лечения даже беременным с легкой гипоксией плода, — говорит Ирина Хабировна Байрамова. — Для преодоления легкой гипоксии, как правило, достаточно просто отдохнуть от забот и перестать нервничать. Но обычно этот совет гинеколога женщины либо игнорируют, либо у них просто нет возможности дома устроить себе полноценный отдых. Прибрать, приготовить, помыть, а еще есть старший ребенок, муж… Планы «полежать отдохнуть вечерком» как правило, срываются…
При лечении гипоксии в условиях стационара проводится терапия, направленная на улучшение снабжения плода кислородом и нормализацию процесса обмена веществ. Если у пациентки с тяжелой гипоксией плода не наблюдается улучшений в течение трех дней, это может свидетельствовать о наличии необратимых изменений в системе «мать-дитя» (например, об отслойке плаценты), и врачи могут принять решение о досрочном родоразрешении на любом сроке беременности (напомним, диагноз «гипоксия» ставится не ранее 28 недели) с целью сохранения жизни ребенка.
— Здоровье большинства женщин, к сожалению, сегодня далеко не идеально, — констатирует Ирина Хабировна Б.айрамова. — Различные хронические заболевания, стрессы, усталость, чрезмерная нагрузка на работе провоцируют различные осложнения беременности. В результате диагноз «плацентарная недостаточность» ставят сегодня каждой второй беременной женщине, «угроза прерывания беременности» — каждой третьей. А если есть плацентарная недостаточность или повышенный тонус матки, значит, есть гипоксия плода. Этот диагноз встречается у 50-70% беременных женщин. Но это не означает, что можно успокоиться тем, что «у всех сейчас так». Ни в коем случае! Напоминания врачей о том, что беременной женщине нужны достаточный сон, отдых, прогулки на свежем воздухе не менее трех часов в день, хорошее питание и витамины, противопоказаны физические, умственные и эмоциональные перегрузки — не пустые слова! Даже имея отклонения в собственном здоровье, женщина может выносить здорового ребенка, если будет придерживаться этих советов. И еще — обследоваться до наступления беременности, чтобы подлечить свои хронические заболевания, исключить или пролечить заболевания, передающиеся половым путем. Крутясь, как белка в колесе в бешеном темпе нашей жизни, остановитесь на секунду и подумайте, что вам важнее — ваша работа (к которой вы еще успеете вернуться, когда малыш подрастет), чистота в доме (к которой можно попробовать относиться проще) или здоровье будущего ребенка? Ведь здоровый или практически здоровый малыш — это огромная экономия жизненных сил, денег и счастье для любой семьи. А девять месяцев — не такой долгий отрезок времени, на который можно попытаться снизить свои нагрузки на любимой работе (например, воспользоваться правом нашего законодательства о сокращении рабочего дня беременной женщины на один час), переложить на кого-нибудь часть забот по дому (или просто забыть о них!) и освоить новое увлечение — медитацию, которое позволит вам расслабляться и успокаиваться, когда эмоции зашкаливают.
Александра Медведева
Развитие детей, перенесших острую и хроническую гипоксию
На правах рукописи —
Пронина Ольга Александровна
РАЗВИТИЕ ДЕТЕЙ, ПЕРЕНЕСШИХ ОСТРУЮ И ХРОНИЧЕСКУЮ ГИПОКСИЮ
14,00.09 — педиатрия
АВТОРЕФЕРАТ
диссертации на соискание ученой степени кандидата медицинских наук
Воронеж — 2009
003469525
Работа выполнена в Государственном образовательном учреждении высшего профессионального образования «Воронежская государственная медицинская академия им. H.H. Бурденко Федерального агентства по здравоохранению и социальному развитию» (ГОУ ВПО ВГМА им. H.H. Бурденко Росздрава)
Научный руководитель: Официальные оппоненты:
Ведущая организация:
доктор медицинских наук, профессор Логвинова Ия Ивановна
доктор медицинских наук, профессор Ситникова Валентина Пантелеевна кандидат медицинских наук Савченко Андрей Пантелеевич
ГОУ ВПО «Волгоградский государственный медицинский университет Федерального агентства по здравоохранению и социальному развитию»
Защита диссертации состоится «2» июня 2009 года в 10°° часов на заседании диссертационного совета Д.208.009.02 при ГОУ ВПО ВГМА им. H.H. Бурденко Росздрава по адресу: 394036, Россия, г. Воронеж, ул. Студенческая, д. 10.
С диссертацией можно ознакомиться в библиотеке ГОУ ВПО ВГМА им. H.H. Бурденко Росздрава
Автореферат разослан «30» апреля 2009 года.
Ученый секретарь диссертационного совета
A.B. Будневский
ОБЩАЯ ХАРАКТЕРИСТИКА РАБОТЫ
Актуальность
Перинатальная гипоксия занимает одно из ведущих мест среди перинатальных факторов, оказывающих влияние не только на состояние плода, но и на особенности течения периода новорожденное™, что, в конечном итоге, сказывается на здоровье и дальнейшем развитии ребенка (Баранов A.A., 2001, Балаболкин И.И., 2003). По данным Барашнева Ю.И. (2005) внутриутробная гипоксия и гипоксия в родах в 38,45% случаев является причиной перинатальной смертности, а в 59,04% — причиной мертворождений. Частота перинатальной гипоксии не имеет тенденции к уменьшению. 60-80% всех заболеваний ЦНС детского возраста связано с перинатальной гипоксией (Бадалян Л.О., 2001). Более половины всех случаев расстройств функций ЦНС у детей раннего возраста обусловлено не острой гипоксией в родах, а длительной, хронической гипоксией плода и новорожденного (Paneth N., 1983, Nelsons К.В., 1996, Volpe J.J., 2008). Значимость проблемы состоит в том, что поражения головного мозга гипоксического генеза определяют неврологическое здоровье и инвалидность с детства (Пальчик А.Б,, 2001; Барашнев Ю.И., 2005). Необходим поиск комплекса современных клинических и лабораторных критериев, позволяющих улучшить раннюю диагностику и прогноз повреждений нервной системы у детей. Своевременное выявление постгипоксических нарушений имеет огромное значение для построения адекватной терапии неврологических расстройств и их профилактики (Барашнев Ю.И., 1991, Баранов A.A., 2006).
На современном этапе развития медицинской науки установлено, что гипоксия, ишемия, ацидоз индуцируют синтез эндотелина-1 (ЭТ-1) (Isozaki-Fukuda Y., 1991, Антонов А.Г., 2006). ЭТ-1 оказывается причастным к сердечно-сосудистой и почечной патологии, диабету (La М., 1995, Gray G., 1996, Pernow J., 1997, Rhoten R., 1997, Schiffrin E.L., 2001, D. Behrendt, 2002, Touyz RM, 2003,), а также участвует в патогенезе легочной гипертензии и постгипоксических нарушений сердечно-сосудистой системы у новорожденных (Kumar Р, 1996, Perreault Т, 2003, Зузенкова Л.В., 2008). Роль ЭТ-1 в развитии перинатальных гипоксических поражений ЦНС и их исходов у новорожденных изучена недостаточно.
В связи с изложенным выше, изучение дальнейшего физического, нервно-психического развития, соматической заболеваемости, оптимизация диагностики и прогнозирования неврологической патологии у детей, перенесших острую и хроническую перинатальную гипоксию, а также изучение роли ЭТ-1 в развитии неврологических расстройств у детей являются весьма актуальными.
Цель исследования
Провести мониторинг развития детей, перенесших острую и хроническую перинатальную гипоксию, а также определить роль ЭТ-1 в
развитии неврологических расстройств гипоксического генеза у детей и выявить наиболее значимые факторы, влияющие на их компенсацию.
Задачи исследования
1. Изучить течение раннего неонатального периода у детей, перенесших острую и хроническую гипоксию.
2. Оценить физическое развитие детей до 3-х лет, перенесших острую, хроническую и сочетанную перинатальную гипоксию.
3. Провести анализ соматической заболеваемости у детей до 3-х лет, перенесших внутриутробную и интранатальную гипоксию.
4. Сравнить неврологические нарушения и сроки их компенсации, в зависимости от вида перенесенной гипоксии.
5. Определить факторы, влияющие на наступление неврологической компенсации после 1,5 лет у детей, перенесших перинатальную гипоксию.
6. Изучить роль ЭТ-1 в развитии неврологических расстройств у новорожденных.
Новизна исследования
Установлены особенности течения раннего неонатального периода, физического развития, соматической заболеваемости у детей, перенесших острую, хроническую и сочетанную гипоксию.
Выявлены особенности неврологических нарушений и сроки их компенсации, в зависимости от вида перенесенной гипоксии.
Определен прогностический вклад факторов, влияющих на позднее наступление неврологической компенсации у детей, перенесших перинатальную гипоксию.
Выявлена диагностическая и прогностическая значимость ЭТ-1 в развитии ХВГП и неврологических нарушений у детей, перенесших внутриутробную гипоксию.
Практическая значимость
Определены особенности течения раннего неонатального периода, физического развития, соматической заболеваемости, неврологических нарушений и сроки их компенсации у детей, в зависимости от вида перенесенной гипоксии.
Установлено, что определение концентрации ЭТ-1 в плазме пуповинной крови и в период ранней неонатальной адаптации у детей с высоким риском хронической внутриутробной гипоксии позволяет судить о наличии постгипоксических нарушений. Показатели ЭТ-1 могут служить критерием раннего прогнозирования развития последствий перинатального поражения ЦНС у детей на первом году жизни.
Выявлено, что для прогнозирования сроков компенсации неврологических расстройств у детей с перинатальной гипоксией (при условии стандартных методов лечения) необходима комплексная оценка
группы факторов, включающих антенатальное развитие и интранатальный период, неонатальную заболеваемость и данные нейросонографии, заболеваемость на протяжении первых 3-х лет жизни.
Предложено комплексное обследование и наблюдение детей, перенесших перинатальную гипоксию, включающее в себя определение ЭТ-1 в пуповинной крови, оценку физического развития с обязательным ежемесячным определением окружностей головы и груди на протяжении 11,5 лет, оценку неврологического и соматического статуса, обязательное проведение нейросонографии не однократно, даже при отсутствии патологии при предыдущих исследованиях. Данный комплекс обследования позволяет выявить в более ранние сроки наличие соматических и неврологических расстройств, а также способствует определению «клинически немых» форм поражения головного мозга и своевременной коррекции выявленных нарушений.
Внедрение в практику
Рекомендации, разработанные на основании полученных в ходе диссертационного исследования данных, используются в учебном процессе на кафедре неонатологии ГОУ ВПО ВГМА им. H.H. Бурденко Росздрава.
Основные положения, выносимые иа защиту:
1. Особенности течения раннего неонатального периода, физического развития, соматической заболеваемости, неврологических нарушений и сроки их компенсации у детей, в зависимости от вида перенесенной гипоксии, необходимо учитывать для профилактики развития постгипоксических нарушений у детей сразу после рождения и в раннем возрасте.
2. Определение концентрации ЭТ-1 в плазме пуповинной крови и в период ранней неонатальной адаптации у детей с высоким риском хронической внутриутробной гипоксии позволяет судить о наличии постгипоксических нарушений. Показатели ЭТ-1 в пуповинной крови могут служить критерием раннего прогнозирования развития последствий перинатальных поражений ЦНС у детей на первом году жизни.
3. Для прогнозирования сроков компенсации неврологических расстройств у детей с перинатальной гипоксией (при условии стандартных методов лечения) необходима комплексная оценка группы материнских факторов и факторов, относящихся к состоянию ребенка.
4. Детям, перенесшим перинатальную гипоксию, необходимо комплексное обследование и наблюдение для выявления в более ранние сроки наличия соматических и неврологических расстройств и своевременной их коррекции.
Апробация работы
Основные результаты работы были представлены на III, V, VI Всероссийских университетских научно-практических конференциях молодых ученых и студентов по медицине (Тула, 2004, 2006, 2007), I Всероссийской Бурденковской студенческой научной конференции (Воронеж, 2005), X конгрессе педиатров России (Москва, 2006), Ежегодной междисциплинарной научно-практической конференции стран СНГ (Санкт-Петербург, 2006), ежегодном конгрессе специалистов перинатальной медицины (Москва, 2006), Первом Объединенном научно-практическом форуме детских врачей (Орел, 2008), И научно-практической конференции «Актуальные вопросы организации, оказания первичной, специализированной медицинской помощи в условиях многопрофильного стационара» (Воронеж, 2008).
Публикации
По материалам диссертации опубликовано 10 работ, две из которых в издании, рекомендованном ВАК РФ.
Объем и структура диссертации
Диссертация изложена на 144 страницах машинописного текста, состоит из введения, обзора литературы, главы, посвященной объекту и методам исследования, трех глав собственных исследований, заключения, выводов, практических рекомендаций, указателя литературы. Работа иллюстрирована 10 рисунками и 37 таблицами, содержащимися в тексте. Библиография содержит 286 источников, в том числе 179 отечественных и 107 иностранных авторов.
ОСНОВНОЕ СОДЕРЖАНИЕ РАБОТЫ
Объект и методы исследования
Проведено обследование 157 детей, В данное исследование были включены дети, перенесшие ХВГП и асфиксию новорожденного, со сроком гестации от 37 до 42 недель, рожденные в роддоме «Электроника» и областном родильном доме в 2002-2005 гг. Критериями исключения новорожденных из исследования стали срок гестации менее 37 недель, травматические повреждения и поражения ЦНС при инфекционных заболеваниях перинатального периода, а также врожденные пороки развития.
Перенесенная детьми гипоксия подтверждалась данными повторных (не менее двух) кардиотокографических и ультразвуковых исследований во 2-м и 3-м триместрах беременности, а также антенатальными и интранатальными факторами риска. Асфиксия новорожденного
устанавливалась согласно критериям диагностики — оценка по шкале Апгар и наличие клинических признаков полиорганных нарушений.
Дети были разделены на пять групп. Первая (контрольная) группа состояла из 30 здоровых доношенных новорожденных, матери которых не имели кардиотокографических признаков страдания плода и ультразвуковых признаков ФПН. Вторую группу составили 25 новорожденных с оценкой по шкале Апгар 4-6 баллов, матери которых также не имели кардиотокографических и ультразвуковых признаков хронической гипоксии плода, т.е. перенесших острую умеренную асфиксию в родах. В третью группу вошло 39 детей с признаками хронической внутриутробной гипоксии плода, не достигающими критических значений. В четвертой группе было 27 новорожденных, перенесших умеренную асфиксию в родах, развившуюся на фоне хронической антенатальной гипоксии. Пятую группу составили 36 детей, рожденных в тяжелой асфиксии на фоне хронической внутриутробной гипоксии плода. Основные характеристики детей представлены в таблице 1.
Таблица 1
1 группа (п=30) 2 группа (п=25) 3 группа (п=39) 4 группа (п=27) 5 группа (п=36)
Мальчики/ Девочки (абс(%) 15/15 (50/50) 17/8 (68/32) 14/25 (36/64) 12/15 (44/56) 21/15 (58/42)
Масса тела при рождении, г (М±а) 3509 ±345 3600 ±398 3247 ±339* 3200 ±289* 3394 ±332
Длина тела при рождении, см (М±сг) 53,1 ±1,7 53,8 ±1,9 51,7 ±2,0 52,3 ±2,5 53 ±2,7
Окружность головы, см (М±ст) 34,6 ±1,0 35,2 ±1,1 34,4 ±1,2 34,6 ±1,4 34,1 ±1,7
Окружность груди, см (М±о) 32,5 ±1,6 33,0 ±1,7 31,9 ±1,6 32,1 ±1,7 32,4 ±1,6
Гестационный возраст, нед (М±о) 39,1 ±0,7 39,5 ±1,0 39,1 ±0,9 38,9 ±0,8 39 ±0,9
Оценка по шкале Апгар 1 мин/5 мин (М±о) 7,0/8,0 5,8±0,5/ 7,0±0,5 7,0/ 7,9±0,2 5,9±0,3/ 7,15±0,4 2,0±0,8/ 4,8±1,3
Примечание: * р<0,01 между группами контроля, «с умеренной асфиксией» и группами «с ХВГП», «с ХВГП+ умеренная асфиксия»
Отмечалось отличие по массе тела в группах детей с перенесенной хронической и сочетанной гипоксией с умеренной асфиксией от контрольной группы и группы детей, перенесших острую умеренную асфиксию. Отличие между группами отмечалось также по тяжести состояния при рождении и оценивалось по шкале Апгар.
Обследование новорожденных в родильном доме включало оценку состояния при рождении по шкапе Апгар, морфофункциональной зрелости
и физического развития, неврологического и соматического статуса, общеклиничекие лабораторные исследования.
Последующее наблюдение за детьми осуществлялось до достижения ими трёхлетнего возраста. Пациентам проводился комплекс клинических, лабораторных и инструментальных исследований в динамике. Все дети были консультированы неврологом, офтальмологом, хирургом.
Оценка физического развития детей в возрасте от 1 месяца до 3-х лет проводилась с использованием центильных таблиц И.М. Воронцова и А.Н. Мазурина соответственно возрасту и полу. Уровень психомоторного развития определялся по методике Л.Т. Журбы и Е.М. Мастюковой (1981), а также с использованием методики В.А. Доскина и соавторов (1997). Ультразвуковое исследование головного мозга проводилось аппаратом «Бшепз 80-450» (Германия), секторными датчиками 3,5 и 7,5 МГц.
С целью изучения состояния функций эндотелия у новорожденных, перенесших ХВГП, была определена концентрация ЭТ-1 в плазме крови у детей со сроком гестации 37-42 недели, рожденных в областном роддоме в 2007 году. Нами был обследован 41 ребенок, которые на основании анамнестических, клинических данных, кардиотокографии и допплерометрии перенесли хроническую внутриутробную гипоксию. Эти дети вошли в основную группу. Группу сравнения составили 12 новорожденных, родившихся у матерей с не осложненным течением беременности и родов. В ходе исследования дети основной группы, перенесшие ХВГП, были разделены на 2 подгруппы. В 1А подгруппу вошло 15 детей, которые в раннем неонатальном периоде не имели признаков гипоксически-ишемического поражения ЦНС. 1Б подгруппу составили 26 детей, имеющие в раннем неонатальном периоде признаки церебральной ишемии I и II степени. Общая характеристика обследуемых пациентов представлена в таблице 2.
Таблица 2
Общая характеристика групп детей, обследуемых на эндотелиальную
дисфункцию
Основная группа Группа сравнения (п=12)
1А подгруппа (п=15) 1Б подгруппа (п=26)
Мальчики/ Девочки (абс(%) 4/11 (27/73) 15/11. (58/42) 6/6 (50/50)
Масса тела при рождении, г (М±о) 3706±224 3246±504* 3615±486
Длина тела при рождении, см (М±сг) 54,2±1,5 52,8±2,1 54±2,8
Окружность головы, см (М±а) 35±1,2 33,9±1,3 35,1±1,4
Окружность груди, см (М±о) 33,6±1,4 32,5±1,5 33,6±1,0
Гестационный возраст, нед (М±о) 39,2±0,9 39,2±0,88 38,8±0,22
Примечание: * р<0,05 между 1А подгруппой, группой сравнения и 1Б подгруппой
Оценка по шкале Апгар у всех детей составила 7-8 баллов. Отмечалось отличие по массе тела в подгруппе детей с церебральной ишемией от контрольной группы и подгруппы без поражения ЦНС.
Количественное определение ЭТ-1 в ЭДТА-плазме производили с помощью иммуноферментного анализа (набор Biomedica).
Последующее наблюдение за детьми, у которых был определен ЭТ-1 в крови, осуществлялось на протяжении первого года жизни с оценкой физического и психомоторного развития, изучением соматической и неврологической патологии, проведением ультразвукового исследования головного мозга.
Статистическая обработка
Статистическая обработка полученных результатов проводилась на персональном компьютере с помощью пакета универсальных программ «Excel» и «Statistica v.6» с использованием общепринятых параметрических и непараметрических методов. Обработка вариационных рядов включала подсчет значений средних арифметических величин (М), стандартной ошибки (ш), стандартного отклонения (а). Частота признаков представлена с указанием стандартной ошибки для качественных признаков, стандартного отклонения для количественных признаков. Для сравнения средних величин количественных переменных использовали t-критерий Стьюдента. Качественные показатели сравнивали по критериям Хи-квадрат и Манна-Уитни. Достоверными считались различия между группами при вероятности ошибки менее 5% (р<0,05). Для выявления взаимосвязей между изучаемыми показателями применяли метод корреляционного анализа, включающий как оценку коэффициента корреляции Спирмена (г), так и уровень его значимости (р). Определение факторов риска поздней (после 1,5 лет) неврологической компенсации проводилось с помощью многомерного регрессионного анализа с 95% доверительным интервалом.
Результаты исследований
Был проведен анализ антенатального, интранатального и раннего постнатального периодов каждого ребенка.
Средний возраст матерей в группах «с ХВГП» (3 группа — 26,33±5,90 лет), «с ХВГП + умеренная асфиксия» (4 группа — 28,48±4,95 лет), «с ХВГП + тяжелая асфиксия» (5 группа — 26,56±6,31 лет) достоверно не отличался между группами и от контроля (1 группа — 27,93±6,06 лет). Средний возраст матерей в группе «с умеренной асфиксией» (2 группа) составил 25,08±3,7б лет и достоверно отличался от контрольной группы и от группы «с ХВГП + умеренная асфиксия» (р<0,05). Следует отметить, что в группе «с ХВГП» и обеих группах с сочетанной гипоксией, а также в контрольной группе, женщины старше 35 лет встречались примерно с одинаковой частотой (в 1, 3, 4 группах — по 5 женщин (16,7%, 12,8%, 18,5% соответственно), в 5 группе — 6 (16,7%) женщин). В группе «с умеренной асфиксией» женщины старше 35 лет не встречались.
Анализ соматической заболеваемости показал, что все женщины до наступления настоящей беременности имели ту или иную соматическую патологию. Во всех группах, включая контрольную, женщины имели высокий процент патологии (69,4% до 96,2%). Осложненный соматический анамнез встречался достоверно чаще только в группе «с ХВГП + умеренная асфиксия» (96,2%), чем во всех остальных (р<0,01). Более половины матерей в группах детей с перенесенной острой и/или хронической гипоксией имели осложненный гинекологический анамнез. В группе «с умеренной асфиксией» преобладали воспалительные (56%), а в группе «с ХВГП» невоспалительные (53,8%) болезни женских половых органов. У матерей в группах «с ХВГП + умеренная асфиксия» и «с ХВГП + тяжелая асфиксия» воспалительные и невоспалительные гинекологические заболевания встречались с одинаковой частотой (по 55,6% и 41,6% соответственно). В контрольной группе осложненный гинекологический анамнез имела четвертая часть женщин. Первая беременность регистрировалась почти у половины женщин в группах контроля, «с ХВГП» и «с ХВГП + тяжелая асфиксия». В группе «с ХВГП + умеренная асфиксия» одна треть детей была рождена от первой беременности. Течение беременности в группах детей с хронической и сочетанной гипоксией (3, 4, 5 группы) осложнилось гестозом второй половины у всех женщин. В 3-й, 4-й и 5-й группах у четверти, одной трети и почти у половины матерей, соответственно, гестоз был в виде нефропатии различной степени. Примерно у половины матерей в этих группах регистрировались анемия беременных, ранний токсикоз и угроза прерывания, каждая пятая женщина перенесла ОРВИ во время беременности. Течение беременности в группе «с умеренной асфиксией» осложнилось более чем у половины матерей анемией беременных, ранним токсикозом, водянкой беременных и угрозой прерывания, которая отмечалась однократно и без длительного лечения, каждая пятая перенесла ОРВИ во время беременности. В контрольной группе однократная угроза прерывания беременности регистрировалась в два раза, водянка беременных в пять раз, а токсикоз в семь раз реже, чем в группах с гипоксией (р<0,001).
Наличие внутриутробного страдания плода подтверждалось проведением КТГ и ультразвуковых допплерометрических исследований. Базальный ритм и ПСП в группах с хронической и сочетанной гипоксией был достоверно выше, чем в 1-й и 2-й группах (р<0,001). В группах с хронической гипоксией и сочетанной умеренной и тяжелой асфиксией выраженное страдание плода отмечалось более чем у половины женщин. В контрольной группе и в группе «с умеренной асфиксией» при кардиотокографическом исследовании патологии не выявлено. Допплерометрическое исследование показало наличие признаков ФПН в группах с хронической и сочетанной гипоксией у всех женщин, тогда как в группе «с умеренной асфиксией» только у 28% беременных (р<0,05). Необходимо отметить, что во 2-й группе встречалась только 1а степень ФПН. В контрольной группе плацентарный кровоток не нарушался.
Самостоятельные роды превалировали в контрольной группе у 66,7% и в группе «с ХВГП» у 53,8% женщин, из них физиологическими были 45% и 23,8% случаев соответственно. В группах «с умеренной асфиксией», «с ХВГП + умеренная асфиксия» и «с ХВГП + тяжелая асфиксия» ни у одной женщины роды не протекали физиологически. Аномалии родовой деятельности в группе «с ХВГП + тяжелая асфиксия» в два раза чаще осложняли течение родов, чем в контрольной группе (р<0,05). Во всех группах с перенесенной гипоксией практически половина родов осложнилась патологией пуповины, что достоверно чаще по сравнению с контролем (р<0,05). Дородовое излитие околоплодных вод в группах «с ХВГП + тяжелая асфиксия» и «с ХВГП» наблюдалось у каждой третьей женщины, что чаще, чем в группах «с умеренной асфиксией» и контроля. Меконий в околоплодных водах встречался примерно у каждой пятой женщины во всех группах с гипоксией.
При анализе течения раннего неонатального периода выявлено, что в контрольной группе наблюдалась низкая заболеваемость. Только у 20% детей встречалась конъюгационная желтуха. В группах с перенесенной гипоксией (2, 3, 4, 5 группы) общая заболеваемость достоверно выше, чем в контрольной группе (р<0,001), и составила от 74,1 до 100%. В 5-й группе наблюдалась самая высокая заболеваемость по сравнению с другими группами (р<0,01). На первом месте во всех группах с перенесенной асфиксией стоят дыхательные и сердечно-сосудистые нарушения, ВЖК также превалировали в этих группах (14-16%). Транзиторное тахипноэ новорожденного достоверно чаще встречалось в 5-й группе, чем в остальных группах с гипоксией (р<0,01). ЗВУР регистрировалась только у детей с хронической гипоксией (3,4, 5 группа) от 14% до 33,3%.
Неврологическая патология в группе «с ХВГП + тяжелая асфиксия» так же, как и соматическая, наблюдалась чаще, чем в других группах. Гипоксическое поражение ЦНС имели все новорожденные этой группы, тогда как во 2-й, 3-й и 4-й группах церебральная ишемия была выявлена у 48%, 38,5%, 59,3% детей соответственно. Ведущим неврологическим синдромом в группах «с умеренной асфиксией», «с ХВГП» и «с ХВГП + умеренная асфиксия» явился гипертензионный синдром (28%, 20,5% и 22,2% соответственно), а в группе «с ХВГП + тяжелая асфиксия» — синдром гипервозбудимости и синдром угнетения (38,9% и 36,1% соответственно). В группе «с ХВГП + тяжелая асфиксия» судорожный синдром встречался у 13,9% детей, а в группе «с умеренной асфиксией» в 4% случаев.
Всем детям были исследованы в капиллярной крови на 1-е и на 5-е сутки концентрация гемоглобина и количество эритроцитов, повышение которых является адаптационным механизмом при кислородной недостаточности. Концентрация гемоглобина и количество эритроцитов на 1-е сутки и количество эритроцитов на 5-е сутки в группе «с ХВГП + тяжелая асфиксия», были достоверно выше, чем в остальных группах. Концентрация гемоглобина на 5-е сутки в группах достоверно не отличалась.
Катамнез детей исследуемых групп
На естественном вскармливании в контрольной группе находилось 76,5% детей, а в группе «с умеренной асфиксией» — 50% детей. Более половины детей в группах с хронической и сочетанной гипоксией вскармливались искусственно (3 группа — 52,3%, 4 группа — 57,1%, 5 группа — 77,8% детей).
При изучении физического развития к вариантам нормы были отнесены характеристики, свойственные 80% популяции и находящиеся в интервале от 10-го до 90-го центиля. К году в группах детей с перенесенной гипоксией от 15% до 50% детей имели дисгармоничное физическое развитие с избытком массы тела. В контрольной группе дисгармоничное физическое развитие с избытком массы тела наблюдалось только у 11,8%. Масса и длина тела ниже 10 центиля на первом году жизни встречалась лишь у детей 4-й (7,1%) и 5-й (5,6%) групп. К трем годам во всех группах отмечалась положительная динамика, кроме группы «с ХВГП», в которой количество детей с гармоничным физическим развитием снизилось до 71,4% (рис. 1).
Длина тела Масса тела
Рис. 1 Физическое развитие детей (длина тела, масса тела)
Окружность груди к году в контрольной группе у всех детей укладывалась в возрастные нормативы. В группе «с ХВГП + умеренная асфиксия» каждый пятый ребенок, а в группе «с ХВГП» более половины детей имели узкую грудную клетку. Показатели окружности головы в контрольной группе в изучаемые возрастные периоды (3 месяца, 1 год) у всех обследуемых укладывались в «коридор» от 10 до 90 центиля. В 4-й группе около половины имели показатели окружности головы ниже 10 центиля. У третьей части детей 5-й группы определялись увеличенные размеры окружности головы. К году в группах с хронической гипоксией и сочетанной умеренной и тяжелой асфиксией положительной динамики не
наблюдалось, только у половины детей показатели окружности головы находились между 10 и 90 центилем (рис. 2).
Окружность головы Окружность груди
Рис. 2 Физическое развитие детей (окружность головы, окружность груди)
Анализируя соматическую патологию у детей, перенесших острую и хроническую гипоксию, в контрольной группе была выявлена более низкая заболеваемость, чем в группах сравнения (р<0,05). В раннем возрасте 70,5% пациентов перенесли ОРВИ, но только в одном случае вирусная инфекция сопровождалась бронхитом. В группах с перенесенной гипоксией все дети переносили ОРВИ в течение трех лет, из них 25% отнесены к группе часто болеющих. В группе «с ХВГП + тяжелая асфиксия» у половины детей, а в группе «с ХВГП + умеренная асфиксия» в 35,7% случаев ОРВИ осложнялась обструктивным бронхитом. Дисбиоз кишечника, атопический дерматит и анемия явились ведущими среди соматической патологии, наиболее часто выявляющиеся в группе с тяжелой асфиксией. Достаточно часто диагностировались астигматизм, конъюнктивиты и отиты в группах детей с гипоксией.
Анализ неврологической заболеваемости в поздний неонатальный период показал, что процент диагностируемых гипоксических поражений ЦНС в группах с перенесенной гипоксией увеличился до 95,2% — 100%. Всем детям в возрасте 1 и 6 месяцев проводилась нейросонография. В контрольной группе на первом месяце жизни только у 17,6% детей наблюдались признаки перивентрикулярного отека. Ликвородинамические нарушения в группе «с умеренной асфиксией» определялись у 16,7% детей, что достоверно реже, чем в группе «с ХВГП + тяжелая асфиксия» (р<0,01). В группах с хронической гипоксией и сочетанной умеренной и тяжелой асфиксией нарушения ликвородинамики выявлено более чем у половины детей. При повторном нейросонографичсском обследовании в 6 месяцев в группе «с ХВГП» процент ликвородинамических нарушений снизился в 1,5
раза по сравнению с предыдущим исследованием и составил 33,3%, что достоверно ниже, чем в группе «с ХВГП + тяжелая асфиксия» (р<0,05). В группах с острой и сочетанной гипоксией (2, 4 и 5 группы) частота встречаемости признаков нарушения ликвородинамики увеличилась до 64,3%-72,2% (рис. 3).
80 70 60 50 40 30 20 10 О
— 80 — 70 60 — 50 40 30 — 20 -■ 10 О
Признаки Признаки
ликвородинамических ликворалниймических нарушений (1 мес) нарушений (б мес)
-«с умеренной асфиксие й «
■ «ХВГП+умерення и асфиксия»
«ХВГП+тнжвлая асфиксия»
Рис. 3 Результаты нейросонографического обследования в 1 и 6 мес
На первом году жизни среди последствий гипоксических поражений ЦНС ведущее место принадлежит доброкачественной внутричерепной гипертензии, которая была диагностирована более чем у половины детей с перенесенной гипоксией. Сочетанные формы задержки развития, расстройства вегетативной нервной системы и церебрастенический синдром регистрировались только в группах с хронической и сочетанной гипоксией (3, 4, 5 группы). В группе «с умеренной асфиксией» нарушение моторного развития выявлялось достоверно реже, чем в группах «с ХВГП» и «с ХВГП + тяжелая асфиксия» у одной трети и в группе с «ХВГП + умеренная асфиксия» у половины детей (р<0,05). У 50% пациентов 5-й группы имелись клинические признаки гипервозбудимости. Одному ребенку в группе «с ХВГП + тяжелая асфиксия» был поставлен диагноз ДЦП. Следует отметить, что в контрольной группе неврологической патологии выявлено не было.
К 3-м годам нарушения моторного развития имел каждый пятый ребенок в группах с хронической и сочетанной гипоксией. Нарушения развития речи и гиперкинетические расстройства отмечались более чем у половины детей в группе «с ХВГП + тяжелая асфиксия», что достоверно чаще по сравнению с группами «с ХВГП» и с «ХВГП + умеренная асфиксия» (р<0,05). Дети 4-й и 5-й групп в 14,3 и 22,2% соответственно имели нарушения сна. У пятой части детей группы «с ХВГП + умеренная асфиксия» выявлена сообщающаяся гидроцефалия (рис. 4). В контрольной группе патология со стороны нервной системы к 3-м годам также не регистрировалась, а в группе «с умеренной асфиксией» наступила компенсация неврологических нарушений к году у всех обследуемых. Дети, перенесшие ХВГП, достигли компенсации неврологических нарушений к 3-м годам.
Расстройства сна (С 47)
■ Ко1гтрольняя группа О «с умеренной асфиксией» □ «с ХВГП» ЕЗ «с ХВГШ-умерениан асфиксия» И «с ХВГП+тижеляя асфиксия» _
Рис. 4 Структура неврологической заболеваемости к 3-м годам
Факторы, влияющие на компенсацию неврологических нарушений
На первом этапе исследования влияния некоторых факторов на сроки компенсации неврологических нарушений были построены корреляционные матрицы изучаемых факторов (61 фактор). В ходе исследования проведен корреляционный анализ для выявления факторов, имеющих высокую степень взаимосвязи. Статистически значимо с поздним (после 1,5 лет) наступлением компенсации неврологических нарушений связаны: кардиотокографические признаки страдания плода с коэффициентом корреляции г = 0,66 (р<0,0001), степень ФПН г = 0,69 (р<0,0001), степень тяжести гестоза г = 0,63 (р<0,0001), интубация трахеи г = 0,51 (р<0,0001), концентрация гемоглобина в первые сутки г = 0,45 (р<0,001), гипоксически-ишемическое поражение ЦНС в раннем г = 0,51 (р<0,0001) и позднем неонатальном периоде г = 0,65 (р<0,0001), диффузные изменения тканей мозга гипоксически-ишемического характера г = 0,49 (р<0,0001) и признаки ликвородинамических нарушений г = 0,51 (р<0,0001) при проведении нейросонографии. Слабая корреляционная связь обнаружена между поздней неврологической компенсацией и частыми ОРВИ г = 0,39 (р<0,001). Отмечена отрицательная взаимосвязь поздней неврологической компенсации с оценкой по шкале Апгар на первой г = -0,56 (р<0,0001) и пятой минуте г = -0,52 (р<0,0001), массой тела г = -0,33 (р<0,001) и окружностью головы при рождении г = -0,31 (р<0,001).
Мы поставили задачу провести сравнительный анализ зависимостей сочетанного воздействия изучаемых факторов с установлением приоритета каждого из них.
В качестве инструментального метода сравнения был использован многомерный регрессионный анализ. Тактика проведения анализа состояла в выявлении статистически значимых зависимостей каждого из изученных
показателей, установлении наиболее «отзывчивых» во влиянии изученных факторов и параметров.
Изучаемые факторы были разбиты на группы:
1. Группа антенатальных и интранатальных факторов:
а) факторы, отражающие соматическую патологию матери;
б) факторы, отражающие течение настоящей беременности;
в) факторы, отражающие период родов;
2. Группа факторов, относящихся к состоянию новорожденного:
а) параметры, характеризующие состояние ребенка при рождении;
б) параметры, характеризующие течение периода новорожденности;
в) параметры, характеризирующие заболеваемость ребенка в раннем
возрасте.
В ходе исследования взаимосвязи соматической патологии матери и сроков компенсации неврологических нарушений, установлено, что ни одно из заболеваний не оказывало значимого влияния на позднюю (после 1,5 лет) неврологическую компенсацию. Суммарный вклад этой группы факторов составил только 4,46% и явился статистически не значимым (р = 0,9308).
Исследуя влияние течения беременности у матери на сроки неврологической компенсации у детей, установлено, что ни один из изучаемых параметров по отдельности не влиял на позднее наступление неврологической компенсации, но в совокупности факторы, отражающие течение настоящей беременности, дали около 53% вклада с вероятностью статистической значимости 99% (р = 0,0000).
При анализе взаимосвязи периода родов и сроков неврологической компенсации у детей, было выявлено, что из всех осложнений интранатального периода только экстренное кесарево сечение влияет на позднюю компенсацию с вероятностью статистической значимости более 95% (р = 0,0401). Суммарный вклад интранатальных факторов составил 14,72% с вероятностью статистической значимости всего 85%.
Общий вклад параметров, характеризующих состояние ребенка при рождении, в позднее наступление неврологической компенсации у детей составил 34% (р = 0,0006). По отдельности ни один из факторов не влиял на сроки неврологической компенсации.
Изучая влияние течения неонатального периода на позднее наступление компенсации неврологических нарушений, выявлена сильная зависимость между сроками компенсации и степенью тяжести церебральной ишемии (р = 0,0486) и синдромом гипервозбудимости (р = 0,0159). Совокупный вклад всех факторов неонатальной заболеваемости составил 50%.
Концентрация гемоглобина на первые (р = 0,0174) и пятые (р = 0,0078) сутки и количество эритроцитов на пятые сутки (р = 0,0315) влияют на сроки неврологической компенсации со статистической значимостью более 95%. Оценка суммарного воздействия этих параметров свидетельствует, что коэффициент детерминации равен 28% с вероятностью 99% (р = 0,0002).
Анализ влияния нейросонографических изменений головного мозга на сроки неврологической компенсации установил, что диффузные изменения тканей мозга гипоксически-ишемического характера (р = 0,0000), перивентрикулярный отек (р = 0,0202) и признаки ликвородинамических нарушений, сохраняющиеся после полугода жизни (р = 0,0001), влияют на позднее восстановление функций после неврологических нарушений у детей с вероятностью до 99%. В совокупности все нейросонографические изменения голоного мозга статистически значимо (р = 0,0000) влияют на время восстановления функций после неврологических нарушений с коэффициентом детерминации 53%.
Среди патологии детей в раннем возрасте значимо влияющим фактором на сроки неврологической компенсации явилась частота ОРВИ (р = 0,0115). Суммарный вклад заболеваемости детей в раннем возрасте в позднюю компенсацию составил 52%. Статистическая значимость сочетанного воздействия указанных факторов составляет 99% (р = 0,0000).
Исследование показателей эндотелина-1 у новорожденных, перенесших хроническую внутриутробную гипоксию
Концентрация ЭТ-1 была определена в крови у 53 новорожденных (41 ребенок основной группы и ¡2 детей группы сравнения). В ходе исследования дети основной группы, перенесшие ХВГП, были разделены на 2 подгруппы. В 1А подгруппу вошло 15 детей, которые в раннем неонатальном периоде не имели признаков гипоксически-ишемического поражения ЦНС. 1Б подгруппу составили 26 детей с признаками церебральной ишемии I и II степени в раннем неонатальном периоде.
На первом этапе исследования маркера эндотелиальной дисфункции у новорожденных был проведен подробный анализ соматической и гинекологической патологии матери, течение настоящей беременности и родов.
Средний возраст матерей в группах достоверно не отличался и составил в контрольной группе 27,75±3,98 лет, в 1А подгруппе — 28,60±5,96 лет, 1Б подгруппе — 27,12±5,64 лет. Анализ экстрагенитальной патологии матерей показал, что различий в общей заболеваемости в группах не обнаружено. В контрольной группе среди экстрагенитальной патологии расстройства вегетативной нервной системы встречались чаще, чем в группе «с ХВГП с церебральной ишемией» (р<0,05). В подгруппах детей с ХВГП преобладали хронический пиелонефрит и расстройства вегетативной нервной системы.
В гинекологическом анамнезе достоверных различий между группами также не выявлено. Во всех группах преобладали воспалительные болезни женских половых органов.
Течение беременности у матерей в группах детей с хронической гипоксией (1А и 1Б подгруппы) осложнилось гестозом второй половины у всех женщин, угрозой прерывания в 1А подгруппе — у одной трети и в 1Б
подгруппе — у половины женщин. В контрольной группе гестоз и угроза прерывания не регистрировались.
Наличие внутриутробного страдания плода подтверждалось проведением КТГ и ультразвуковых допплерометрических исследований. ПСП, частота встречаемости ФПН и маловодие в группах с хронической гипоксией было достоверно выше, чем в контрольной (р<0,001). В 1Б подгруппе выраженное страдание плода отмечалось более чем у половины женщин, тогда как в 1А только у трети обследуемых. В контрольной группе при кардиотокографическом исследовании патологии не выявлено. Допплерометрическое исследование показало наличие признаков ФПН в грушах с хронической гипоксией у всех женщин. В контрольной группе у половины беременных встречалась только 1а степень ФПН.
Течение интранатального периода в группах не отличалось. Путем самостоятельных родов было рождено более половины детей во всех группах. Аномалии родовой деятельности и патология пуповины осложнили течение родов у одной трети женщин в группах с ХВГП. Дородовое излитие околоплодных вод в группе «с ХВГП с церебральной ишемией» наблюдалось у каждой пятой женщины. В контрольной группе более половины самостоятельных родов протекали физиологически.
Отсутствие достоверных различий в соматической и генитальной патологии у матерей, а также отличий по полу, сроку гестации, оценке по шкале Апгар у детей во всех исследуемых группах позволило нам провести сравнение показателей ЭТ-1 в подгруппах с ХВГП и оценить участие маркера эндотелиальной дисфункции в неонатальной заболеваемости. Для этого концентрация ЭТ-1 была определена у новорожденных в пуповинной крови и на 3-5 сутки (таблица 3).
Таблица 3
Содержание ЭТ-1 в плазме крови новорожденных сразу после рождения
и на 3-5 день жизни
Контрольная группа (п= 12) Основная группа (п=41)
1А(п=15) 1Б (п=26)
ЭТ-1 в плазме пуповинной крови, фмоль/мл 0,81±0,21 2,21±0,66* 1,93±0,87*
ЭТ-1 в плазме на 3-5 сутки, фмоль/мл 1,14±0,42 1,62*0,49″» 1,51*0,49*’
Примечание: * р<0,001 между контрольной группой и группами с ХВГП
*1 р<0,05 между контрольной группой и группами с ХВГП
При анализе полученных данных было выявлено достоверное повышение ЭТ-1 в пуповинной крови как в 1А подгруппе — 2,21±0,17 фмоль/мл, так и в 1Б — 1,93±0,17 фмоль/мл, по сравнению с контрольной группой (р<0,001). Определение уровня ЭТ-1 в крови новорожденных детей в период ранней неонатальной адаптации на 31-5 сутки показало, что произошло его незначительное снижение, но все-таки он оставался
достоверно повышен 1,62±0,16 фмоль/мл в 1А подгруппе и 1,51 ±0,11 фмоль/мл в 1Б, по сравнению с контрольной группой (р<0,05). Вероятно, повышение маркера эндотелиальной дисфункции явилось следствием постгипоксических нарушений у детей в ранний неонатальный период.
Соматическая патология в раннем неонатальном периоде в подгруппе 1Б встречалась чаще, чем в других группах. ЗВУР регистрировалась практически у половины новорожденных в подгруппе 1Б, каждый пятый перенес транзиторное тахипноэ, постгипоксическая кардиолатия и ВУИ были обнаружены по 15,4% случаев. В подгруппе без гипоксического поражения ЦНС были выявлены конъюгационная желтуха у пятой части детей и транзиторное тахипноэ в 13,3% случаев. В контрольной группе превалировали анемия, конъюгационная желтуха и транзиторное тахипноэ у детей рожденных путем кесарева сечения с одинаковой частотой (16,7%).
Критерием включения детей в 1Б подгруппу явилась церебральная ишемия. 1 и II степень тяжести этой патологии встречалась одинаково часто. Синдром гипервозбудимости был определен ведущим и составил 65,4% случаев среди всех неврологических синдромов. Гипертензионный синдром и синдром угнетения регистрировались у пятой части детей, в меньшем проценте (11,5%) встречался синдром вегето-висцеральных дисфункций (рис.5). ________
О Синдром
гипс рвозбуди мости
И Синдром
■ Синдром всгето-висцеральных дисфункций Ш Гипертеизион мый синдром
Рис. 5 Клинические синдромы церебральной ишемии в подгруппе «с ХВГП с церебральной ишемией»
Для выявления участия ЭТ-1 в формировании гипоксического поражения ЦНС было прослежено дальнейшее развитие на первом году жизни у 28 детей.
Показатели физического развития к году у детей в контрольной группе и 1А подгруппе находились между 10 и 90 центилем. В подгруппе «с ХВГП с церебральной ишемией» практически половина детей (41,7%) имели окружность груди ниже 10 центиля, и только у одного ребенка значения роста к году были ниже 10 центиля. Окружность головы на первом году жизни в контрольной группе соответствовала 10-90 центилю у всех обследуемых. Увеличение размеров окружности головы в первом полугодии произошло на 6,9±0,83 см, что соответствовало возрастной норме. Темпы роста окружности головы в первом полугодии у детей основной группы (8,4±1,3 см и 9,2±1,9 см в 1А и 1Б подгруппах соответственно) достоверно выше, чем в контрольной группе (р<0,01).
Всем детям в возрасте 1 месяца проводилась нейросонография. В контрольной группе патологии не было выявлено. В подгруппе «с ХВГП без церебральной ишемии» на первое место выступали перивентрикулярный отек и диффузные изменения тканей мозга гипоксически-ишемического характера по 75% случаев. Эти же изменения в головном мозге у детей подгруппы «с ХВГП с церебральной ишемией» встречались также более чем у половины обследуемых. Более половины детей 1Б подгруппы имели признаки ликвородинамических нарушений, тогда как в 1А признаки нарушения ликвородинамики визуализированы в 37,5% случаев.
При неврологическом обследовании в 1А подгруппе клинические признаки последствий перинатального поражения ЦНС были обнаружены у всех детей, проявляющиеся у 75% нарушением моторного развития, у одной трети — сочетанными формами задержки развития. У половины обследуемых обнаружен гипертензионный синдром. В 1Б подгруппе последствия церебральной ишемии выявлены у 9 пациентов (75%). Среди неврологической патологии в этой подгруппе превалировали сочетанные формы задержки развития (66,7%). Нарушения моторного развития и гипертензионный синдром встречались с одинаковой частотой (по 58,3%)
Рис. 6 Неврологическая патология у детей на первом году жизни
Нужно отметить, что неврологическая патология наблюдалась в группах с ХВГП у детей, Которые имели в раннем неонатальном периоде уровень ЭТ-1 выше, чем максимальное значение у детей в контрольной группе (1,1 фмоль/мл) (рис. 7).
I □ частоте
встречаемости последствий иереребральной ишемии
концентрация ЭТ-1 в пуповинной крови, фмоль/мл
Рис. 7 Частота встречаемости последствий
церебральной ишемии в зависимости от концентрации эндотелина-1
Учитывая, что симптомокомплекс при таких нозологических формах, как нарушение моторного развития и сочетанные формы задержки развития имеет диагностическое значение при исключении других причин, был проведен анализ соматической патологии. Во всех группах на первое место выступали ОРВИ от 62,5% до 83,3%, но в группу часто болеющих не был включен ни один ребенок. У одной трети детей основной группы встречалась анемия, у четверти пациентов — дисбиоз кишечника и атопический дерматит. В контрольной группе процент соматической патологии был ниже, однако, достоверных отличий в заболеваемости детей контрольной и основной групп выявлено не было.
При проведении корреляционного анализа обнаружена прямая взаимосвязь концентрации эндотелина-1 в пуповинной крови с хроническим пиелонефритом у матери с коэффициентом корреляции г = 0,6 (р<0,001), гестозом г = 0,55 (р<0,001), инфекционными заболеваниями матери во время беременности г = 0,65 (р<0,001), концентрацией гемоглобина г = 0,67 (р<0,001) и количеством эритроцитов г = 0,59 (р<0,001) у новорожденных в крови на 1-е сутки. Статистически значимо с концентрацией ЭТ-1 в период ранней неонатальной адаптации связаны многоводие г = 0,58 (р<0,001), кардиотокографические признаками страдания плода г = 0,67 (р<0,001), ВУИ г = 0,58 (р<0,001). Проведенный корреляционный анализ выявил также прямую зависимость между концентрацией эндотелина-1 в пуповинной крови и на 3-5 сутки и диффузными изменениями тканей мозга гипоксически-ишемического характера с коэффициентом корреляции г =
0.67 (р<0,001) и г = 0,56 (р<0,001), сочетанными формами задержки развития г = 0,53 (р<0,001) и г = 0,74 (р<0,0001), нарушением моторного развития г = 0,59 (р<0,001) и г = 0,58 (р<0,001) соответственно. Доброкачественная внутричерепная гипертензия коррелирует только с концентрацией ЭТ-1 на 3-5 сутки г = 0,67 (р<0,001).
На основании изложенного выше, можно сделать вывод, что дети, перенесшие хроническую внутриутробную гипоксию, имеют повышенные показатели ЭТ-1 как в плазме пуповинной крови, так и в плазме крови на 35 сутки. Увеличение уровня ЭТ-1 в крови сохраняется независимо от наличия клинических проявлений, что говорит о сохраняющихся в организме новорожденного постгипоксических нарушениях и о развитии эндотелиальной дисфункции, что впоследствии приводит к неврологическим нарушениям на первом году жизки.
ВЫВОДЫ
1. В раннем неонатальном периоде у трети детей с ХВГП в сочетании и без асфиксии встречалась ЗВУР. У новорожденных, перенесших асфиксию острую или на фоне ХВГП, преобладали дыхательные, сердечно-сосудистые нарушения и ВЖК гипоксического генеза. Наименьший процент
церебральной ишемии приходился на детей, перенесших только хроническую гипоксию.
2. Дисгармоничное физическое развитие с избытком массы тела у детей, перенесших острую и хроническую гипоксию, к году составило от 15% до 50%. Более половины детей с ХВГП в возрасте одного года имели узкую грудную клетку. Только у половины детей с ХВГП в сочетании и без асфиксии окружность головы соответствовала возрастным нормативам. Гармоничное физическое развитие к трем годам реже встречалось у детей, перенесших только ХВГП.
3. При анализе соматической заболеваемости установлено, что от 20% до 30% детей, перенесших острую, хроническую или сочетанную гипоксию, относятся к группе часто болеющих. Анемия, дисбиоз кишечника и атопический дерматит являются преобладающими в структуре заболеваемости.
4. В структуре неврологической заболеваемости на первом году жизни превалировали доброкачественная внутричерепная гипертензия, а к 3-м годам нарушения развития речи и гиперкинетические расстройства. Дети, перенесшие умеренную острую асфиксию, достигли компенсации неврологических нарушений к году, а дети с ХВГП, к 3-м годам. У пятой части детей с тяжелой асфиксией и у одной трети детей с умеренной асфиксией, развившихся на фоне ХВГП, компенсация неврологических нарушений к 3-м годам не наступила. Частота развития ДЦП составила 5,6%.
5. При изучении факторов риска поздней (после 1,5 лет) неврологической компенсации установлено, что наиболее высокая доля вклада принадлежит течению настоящей беременности, патологическим изменениям в головном мозге при нейросонографии и заболеваемости детей в течение 3-х лет (коэффициент детерминации = 53%). Суммарная доля неонатальной заболеваемости составила 50% вклада, а состояние ребенка при рождении -34% вклада.
6. Показатели ЭТ-1 у детей, перенесших хроническую внутриутробную гипоксию, являются повышенными как в пуповинной крови, так и на 3-5 сутки. У детей с ХВГП, имеющих уровень ЭТ-1 в пуповинной крови выше, чем максимальное значение у детей в контрольной группе развиваются неврологические нарушения на первом году жизни. Таким образом, ЭТ-1 можно считать маркером хронической внутриутробной гипоксии, имеющим прогностическое значение в развитии неврологических нарушений.
ПРАКТИЧЕСКИЕ РЕКОМЕНД АЦИИ
1. Для прогнозирования сроков компенсации неврологических расстройств у детей с перинатальной гипоксией (при условии стандартных методов лечения) необходима комплексная оценка группы факторов, включающих антенатальное развитие и интранатальный период, неонатальную заболеваемость и данные нейросонографии, заболеваемость на протяжении первых 3-х лет. Обследование и
наблюдение детей, перенесших перинатальную гипоксию, должно включать в себя оценку физического развития с обязательным ежемесячным определением окружностей головы и груди на протяжении 1-1,5 лет, оценку неврологического и соматического статуса, обязательное проведение нейросонографии всем детям в первом полугодии жизни не менее 2-х раз, даже при отсутствии патологии при предыдущем исследовании. Данный комплекс обследования позволяет выявить в более ранние сроки наличие соматических и неврологических расстройств, а также способствует определению «клинически немых» форм поражения головного мозга, что определяет своевременную коррекцию выявленных нарушений.
2. Рекомендовано внедрить в практическую медицину определение концентрации ЭТ-1 в плазме пуповинной крови у детей с высоким риском хронической внутриутробной гипоксии для выявления наличия постгипоксических нарушений и раннего прогнозирования развития последствий перинатального поражения ЦНС у детей на первом году жизни.
Список работ опубликованных по теме диссертации:
1. Катамнез детей, перенесших тяжелую асфиксию в родах У O.A. Дрожжина, Л.И. Ипполитова, С.Л. Хачатурян, A.M. Якунинская, Е.В. Минакова // Пути повышения эффективности медицинской помощи детям: материалы X конгресса педиатров России. — М., 2006. — С. 186.
2. Физическое развитие и заболеваемость детей, перенесших тяжелую асфиксию в родах / O.A. Дрожжина, Л.И. Ипполитова, С.Л. Хачатурян, А.М, Якунинская, Е.В. Минакова // Сборник материалов 5 Всероссийской университетской научно-практической конференции молодых ученых и студентов по медицине. — Тула, 2006. — С. 88 — 89.
3. Оценка физического развития и структуры заболеваемости детей, перенесших тяжелую асфиксию в родах / O.A. Дрожжина, Л.И. Ипполитова, С.Л. Хачатурян, A.M. Якунинская, Е.В. Минакова // Перспективы и пути развития неотложной педиатрии: материалы ежегодной междисциплинарной научно-практической конференции стран СНГ. — Санкт-Петербург, 2006. — С. 69 — 70.
4. Дрожжина O.A. Развитие и структура заболеваемости детей, перенесших тяжелую асфиксию / O.A. Дрожжина // Новые технологии в перинатологии: материалы ежегодного конгресса специалистов перинатальной медицины. — М., 2006. — С. 22.
5. Пронина O.A. Катамнез развития детей, перенесших тяжелую асфиксию интранатально / O.A. Пронина, И.И. Логвинова // Сборник материалов VI Всероссийской университетской научно-практической конференции молодых ученых и студентов по медицине. — Тула, 2007. — С. 204 — 205.
6. Пронина O.A. Исследование показателей эндотелина-1 у новорожденных детей, перенесших хроническую внутриутробную гипоксию / O.A.
Пронина // Системный анализ и управление в биомедицинских системах. — 2008. — Т 7, № 3. — С. 691 — 693.
7. Эндотелии-1 — маркер внутриутробной гипоксии у новорожденных детей / O.A. Пронина, И.И. Логвинова, Л.И. Ипполитова, Л.П. Лободина, Н.П. Стасенкова // Вестник Российского государственного медицинского университета. — 2008. — № 4 (63). — С. 164.
8. Концентрация плазменного эндотелина у новорожденных с перинатальным гипоксическим поражением центральной нервной системы / O.A. Пронина, И.И. Логвинова, М.В. Сулина, Т.Г. Чистотинова, Е.В. Трухачева, Н.В. Заяц // Актуальные вопросы организации, оказания первичной, специализированной медицинской помощи в условиях многопрофильного стационара: материалы II научно-практической конференции, посвященной 130-летию родильного дома ГКБСМП № 10. — Воронеж, 2008. — С. 54 — 57.
9. Пронина O.A. Эндотелиальная дисфункция у новорожденных детей, перенесших хроническую внутриутробную гипоксию / O.A. Пронина, И.И. Логвинова // Современная перинатология: организация, технологии и качество: материалы 3 ежегодного конгресса 6 съезда Российской ассоциации специалистов перинатальной медицины. — 2008. — С. 43.
10. Роль эндотелина-1 в развитии церебральной ишемии у новорожденных / О.А, Пронина, И.И. Логвинова, Л.П. Лободина, Н.П. Стасенкова, Т.Г. Чистотинова // Современные технологии в педиатрии и детской хирургии: материалы VII Российского конгресса. — 2008. — С. 198 — 199.
СПИСОК СОКРАЩЕНИЙ
ВЖК — внутрижелудочковое кровоизлияние ВУИ — внутриутробная инфекция ДЦП — детский церебральный паралич ЗВУР — задержка внутриутробного развития КТГ — кардиотокография
ОРВИ — острая респираторная вирусная инфекция
ПСП — показатель состояния плода
ФПН — фето-плацентарная недостаточность
ХВГП — хроническая внутриутробная гипоксия плода
ЦНС — центральная нервная система
ЭТ — эндотелии
Подписано в печать 15.04.2009 г. Формат 60 х 84/16 . Бумага офсетная. Усл. печ. л. 1,4 Тираж 101 экз. Заказ № 1162
Отпечатано в типографии Воронежский ЦНТИ-филиал ФГУ «Объединение «Росинформресурс» Минпромэнерго России
394730, г. Воронеж, пр. Революции, 30
Родовая травма: гипоксия
Гипоксия возникает, когда ребенок получает недостаточное количество кислорода в мозг до, во время или после родов. Состояние может привести к травме головного мозга и, при неправильном лечении, может перерасти в постоянное расстройство, такое как церебральный паралич, когнитивные нарушения или гипоксически-ишемическая энцефалопатия (ГИЭ). Однако гипоксия не обязательно приводит к стойкой инвалидности. В то время как большинство детей, рожденных с легкой гипоксией, выздоравливают без постоянной инвалидности, умеренная или тяжелая гипоксия значительно увеличивает риск того, что у вашего ребенка будет пожизненная инвалидность.
Что вызывает гипоксию?
Чем дольше его не лечить, тем больше вероятность того, что гипоксия приведет к необратимой инвалидности. Поэтому очень важно как можно скорее выявить гипоксию. Гипоксия новорожденных может возникнуть в любое время до, во время или после родов. К потенциальным факторам риска гипоксии относятся:
- Инфекция
- Травмы пуповины
- Плацентарная недостаточность — нарушение кровотока, приводящее к недостаточному росту плаценты
- Врожденный порок сердца
- Отслойка плаценты — слизистая оболочка плаценты отделяется от матки матери
- Сердечно-сосудистый коллапс
- Выпадение пуповины — пуповина выходит из матки раньше или одновременно с плодом
- Кислородная депривация
- Дистоция плеча — плечо ребенка застревает за лобковой костью матери во время родов
- Патология кровеносных сосудов головного мозга
Варианты лечения
Первым шагом в лечении является реанимация младенца и стабилизация потока кислорода.После этого, в зависимости от потребностей ребенка, лечение может включать лечение гипо- или гипертермии, введение жидкости и обеспечение адекватной вентиляции. В последние годы популярным методом лечения стала охлаждающая терапия. Охлаждающая терапия включает в себя пластиковое одеяло, в которое циркулирует холодная вода. Охлаждающая терапия обычно длится менее трех дней, и в течение этого времени она замедляет отек мозга и гибель клеток, что в противном случае привело бы к необратимому повреждению мозга.
Если гипоксия переросла в необратимую травму головного мозга с когнитивным дефицитом, церебральным параличом или другими результатами, тогда лечение сосредотачивается на сочетании лекарств и долгосрочной терапии. Постоянное повреждение головного мозга, вызванное продолжительной гипоксией, неизлечимо, поэтому лечение обязательно должно длиться всю жизнь. Затраты на пожизненную биологическую и психологическую терапию (и дополнительные затраты на поддерживающую терапию) часто непомерно высоки. Семьям также может потребоваться какая-либо форма психологической терапии, чтобы помочь справиться с эмоциональным и финансовым бременем, с которым они сталкиваются.
Медицинская халатность и правовые средства правовой защиты
В случае гипоксии травма происходит быстро, но ее можно предотвратить, а это означает, что, если будут приняты правильные меры, часто можно избежать постоянной инвалидности. Учитывая успехи, достигнутые в выявлении и лечении гипоксии за последние пятнадцать лет, гипоксия, переходящая в необратимую травму, может быть результатом медицинской халатности со стороны врача или других медицинских работников. Согласно закону о врачебной халатности, медицинские работники должны придерживаться действующих стандартов, чтобы гарантировать выявление любого недомогания и своевременное лечение.Если врач не соблюдает эти стандарты и в результате ребенок получает необратимую травму, врач может быть привлечен к ответственности за врачебную халатность.
Получите юридическую помощь по иску о травме, вызванной гипоксией
После травмы ребенка родители хотят думать только о том, чтобы помочь своему ребенку. После получения необходимой информации, лечения и поддержки от вашего врача следующим шагом может быть получение необходимой вам юридической помощи. Если вы считаете, что травма вашего ребенка могла быть вызвана халатностью медицинского работника, вы можете начать с обсуждения вашего дела с квалифицированным поверенным по врачебной халатности.
Гипоксия плода | Адвокаты Сиракуз по вопросам медицинской халатности DeFrancisco & Falgiatano, LLP
Опытные поверенные по родовым травмам, помогающие семьям в северной части штата Нью-Йорк
Часто дистресс плода выявляется по аномальной частоте сердечных сокращений плода. Он используется для описания плода, не получающего достаточно кислорода во время беременности или родов. Плод может быть лишен достаточного количества кислорода по ряду причин, включая курение матери, низкий уровень кислорода в крови матери, выпадение пуповины или инфаркт плаценты.Иногда задержка внутриутробного развития плода вызывается гипоксией плода или является ее следствием. Если ваш ребенок получил родовые травмы из-за гипоксии плода, которая не была должным образом устранена или обращена врачом в Сиракузах, Рочестере или за его пределами, вы можете взыскать убытки с поставщика медицинских услуг. В DeFrancisco & Falgiatano наши юристы по фетальной гипоксии в Сиракузах гордятся тем, что обеспечивают надежное юридическое представительство по искам наших клиентов против небрежных поставщиков медицинских услуг.
Претензии, возникающие в результате гипоксии плода
И «асфиксия», и «гипоксия» используются для описания неадекватного поступления кислорода к ребенку до, во время или сразу после рождения.Признаки того, что ребенку не хватает кислорода, включают неустойчивую или пониженную частоту сердечных сокращений плода и отсутствие движений. Есть разные причины гипоксии плода. Во-первых, у матери есть заболевание, при котором снижается уровень кислорода в крови. Другая проблема заключается в том, как плацента обеспечивает кислород.
Однако в некоторых случаях врачебная халатность приводит к родовой травме или осложнению родов, например дистоции плеча, которая снижает количество кислорода, которое получает ребенок. Например, врач может чрезмерно стимулировать матку с помощью слишком большого количества питоцина.Медсестра может не контролировать кровяное давление матери. Или врач может не вызвать роды у матери, страдающей гестационным диабетом, что позволит ей умереть после свидания, и плацента может перестать функционировать. Результатом может стать гипоксия плода. Признаки при рождении включают посинение или бледность кожи, более низкую частоту сердечных сокращений, ослабленный мышечный тонус, более слабый крик, плохие рефлексы и затрудненное дыхание. Если вы заметили какой-либо из этих признаков, вам следует обратиться к поверенному по поводу гипоксии плода в районе Сиракуз, который может расследовать ситуацию.
Когда гипоксия плода не лечится или не лечится должным образом, это может привести к травме головного мозга, церебральному параличу, когнитивным проблемам, гипоксической ишемической энцефалопатии или даже смерти. Умеренная или тяжелая гипоксия плода существенно увеличивает риск пожизненной инвалидности у ребенка. Не существует лекарства от повреждения мозга, вызванного умеренной или тяжелой гипоксией, а затраты на лечение этих состояний непомерно высоки — часто намного больше, чем ожидают новые родители за новорожденного или ребенка.Семьям часто требуется терапия, чтобы справиться с проблемами ухода за ребенком с когнитивными проблемами или повреждениями головного мозга. Можно привлечь к ответственности врача, если врачебная халатность вызывает гипоксию плода и родовые травмы.
Если вам необходимо установить врачебную халатность для возмещения повреждений после того, как у вашего ребенка разовьется гипоксия плода, ваш поверенный по гипоксии плода в Сиракузах должен будет доказать, что скорее всего, чем маловероятно, были отношения между врачом и пациентом, врачом или другим лицом. Медицинский работник отклонился от принятых профессиональных стандартов в отношении таких пациентов, как мать и ребенок, в определенной географической области, и это отклонение привело к тому, что ваш ребенок получил травмы.Когда врачу не удается справиться с гипоксией плода должным образом и в соответствии с тем, как с ней справились бы другие поставщики медицинских услуг, находящиеся в аналогичном положении, он может нести ответственность за причиненный ущерб.
Ущерб, который вы можете возместить от имени своего ребенка, включает лечение, медицинское оборудование, лекарства, стоимость пожизненного и реабилитационного ухода, терапию, боль и страдания, а также потерянное удовольствие от жизни. Вы также можете возместить ущерб, причиненный вашим эмоциональным расстройством, когда гипоксия плода ребенка приводит к серьезным эмоциональным расстройствам для другого родителя ребенка и вас.
Найдите юриста по фетальной гипоксии в Сиракузах или окрестностях
Роды должны быть радостным временем. Однако для родителей, чьи дети страдают родовыми травмами, это может быть время огромного стресса, поскольку они пытаются решить, как справиться с такими проблемами, как чрезмерно дорогостоящее лечение или необходимость в уходе на протяжении всей жизни. Если ваш ребенок получил травмы из-за того, что врач не смог должным образом справиться с гипоксией плода, наша юридическая фирма может помочь вам взыскать убытки с ответственных сторон.Мы также представляем семьи в Рочестере, Бингемтоне, Оберне, Эльмире, Норвиче, Кортленде, Дели, Херкимере, Уотертауне, Ловилле, Онейде, Вампсвилле, Ютике, Канандаигуа, Освего, Куперстауне, Итаке, Лионе и во всех северных районах штата Нью-Йорк. Позвоните нам по телефону 315-479-9000 или свяжитесь с нами через нашу онлайн-форму.
Продолжительные роды могут вызвать асфиксию при рождении и повреждение мозга
Асфиксия при рождении и ГИЭ: определения
Асфиксия при рождении возникает, когда младенец испытывает недостаток кислорода в мозгу во время или почти во время рождения.Гипоксическая ишемическая энцефалопатия (ГИЭ) — это повреждение головного мозга, вызванное недостатком кислорода в крови и снижением кровотока в головном мозге. Асфиксия при рождении и ГИЭ могут вызвать у ребенка необратимое повреждение головного мозга, которое может привести к долгосрочным состояниям, таким как церебральный паралич, судорожные расстройства, задержка в развитии и неспособность к обучению. Асфиксию при рождении и ГИЭ часто можно предотвратить, внимательно наблюдая за ребенком и быстро доставив его при первых признаках или надвигающемся стрессе. Квалифицированные члены медицинской бригады будут знать о дистрессе, если они будут постоянно просматривать записи сердечного ритма ребенка на датчике сердечного ритма плода.Кроме того, определенные условия повышают вероятность дистресса, и медицинская бригада должна следить за матерью и ребенком в таких опасных ситуациях. Например, тазовое предлежание повышает вероятность выпадения пуповины, а цефалопазовая диспропорция (ребенок слишком большой для размера таза матери) увеличивает риск родовой травмы и асфиксии. Поставка кесарева сечения составляет , требуется для CPD и большинства типов тазового предлежания.
Спикер на открытии программы «Помощь младенцам в дыхании» (которая является партнером Американской академии педиатрии) отметил, что тяжелые родовые травмы, вызванные асфиксией при рождении и ГИЭ, продолжительными родами и затрудненными родами, часто возникают из-за отсутствия у медицинских работников необходимых навыков. для предотвращения травм.
Как продолжительные роды вызывают асфиксию при рождении и ГИЭ (гипоксическую ишемическую энцефалопатию)?
Роды обычно считаются продолжительными, если первый и второй вместе взятые периоды родов продолжаются более 20 часов для первой беременности и более 14 часов для женщин, родивших ранее. Длительные и задержанные роды в основном имеют 2 причины: неадекватные схватки и / или механические препятствия, такие как ненормальное предлежание ребенка.
Роды обычно считаются продолжительными, если первый и второй вместе взятые периоды родов продолжаются более 20 часов для первой беременности и более 14 часов для женщин, родивших ранее.
К аномальным представлениям относятся следующие:
- Ягодичное предлежание, при котором сначала ноги или ягодицы ребенка видны
- Изображение лица, на котором лицо ребенка готово выйти из родовых путей в первую очередь
- Отклоненное положение головы, при котором шея ребенка менее согнута, прямая или вытянутая
- Положение ребенка в матке таково, что голова ребенка выходит вперед и наклонена к плечу, из-за чего голова ребенка больше не совпадает с родовыми путями (асинклитизм).
Головно-тазовая диспропорция (ЦФ) — еще одно состояние, которое может привести к затягиванию или остановке родов. CPD возникает, когда размер головы ребенка больше, чем размер родовых путей матери, или когда ребенок находится в положении, которое не позволяет ему перемещаться по родовым путям.
Аномальные предлежания и CPD повышают риск многочисленных осложнений, таких как пролапс / компрессия пуповины, что может вызвать тяжелую асфиксию при рождении и ГИЭ. Кроме того, некоторые из этих событий увеличивают вероятность того, что врач попытается ускорить роды, используя опасные для родов препараты Pitocin и Cytotec или опасные устройства для родов, такие как щипцы и вакуумные экстракторы.Часто эти лекарства и устройства фактически продлевают роды, потому что врач полагается на них, вместо того, чтобы перейти к немедленному родоразрешению. В самом деле, очень опасно пытаться принудительно родить через естественные родовые пути, особенно когда существуют CPD и определенные положения ягодичного предлежания, требующие родоразрешения с использованием кесарева сечения. Младенцы, испытывающие затяжные или приостановленные роды, могут начать испытывать асфиксию при рождении и ГИЭ из-за проблем с пуповиной или стресса, связанного с слишком частыми схватками.
Недостаточная активность матки — наиболее частая причина продолжительных и задержанных родов.Это относится к активности матки, которая либо недостаточно сильна, либо не скоординирована должным образом для расширения шейки матки и изгнания ребенка. Мышца матки может не сокращаться должным образом, когда она сильно растянута, как при беременности двойней и гидрамнионе (избыток околоплодных вод). Наличие опухолей в мускулатуре матки также может повлиять на сокращение матки.
Неадекватные сокращения обычно лечат стимуляцией матки. Обычно это достигается с помощью Cytotec или Pitocin.Эти препараты могут вызывать чрезмерные схватки, называемые гиперстимуляцией, которые могут травмировать ребенка. Когда схватки слишком быстрые и сильные, плацента, которая помогает переносить богатую кислородом кровь к ребенку, часто не может восполнить запасы этой крови для ребенка. По мере продолжения гиперстимуляции кислородное голодание ребенка прогрессивно ухудшается. Действительно, использование Pitocin или Cytotec требует очень тщательного наблюдения за частотой сердечных сокращений ребенка, и ребенок должен быстро родиться при первых признаках дистресса.
Чрезмерное употребление обезболивающих или анестезии может вызвать неэффективную деятельность матки и может помешать матери добровольно родить ребенка во втором периоде родов. Исследования показывают, что анестезия может увеличить продолжительность второго периода родов и что она увеличивает использование питоцина, а также частоту использования щипцов и вакуум-экстрактора.
В этом видео медсестра Андреа Ши рассказывает о ненормальных режимах родов.
Дистоция или стеноз шейки матки
Термин «цервикальная дистоция» используется, когда шейка матки не раскрывается должным образом и остается в том же положении более 2 часов после латентной фазы родов.Шейка матки может не расширяться, если она фиброзирована из-за предыдущих операций, таких как коническая биопсия (тип биопсии шейки матки, при которой удаляется конусообразный кусок ткани), или из-за наличия опухолей. Врачи должны знать об этих проблемах у матери и ожидать возможности продолжительных или остановленных родов и необходимости срочного родоразрешения.
Дистоция плеча — еще одна очень рискованная ситуация. Это происходит, когда плечо ребенка застревает в тазовой кости матери во время родов.Есть определенные приемы, которые врач может предпринять, чтобы попытаться освободить плечо, чтобы можно было родить ребенка. Однако это может привести к травме головы и другим травмам. Иногда врачи могут слишком сильно тянуть ребенка за голову, пытаясь вытащить его из родовых путей. Это противоречит стандартам ухода, поскольку чрезмерное усилие может привести к растяжению и разрыву нервов шеи и плеч ребенка, что может вызвать паралич руки или паралич Эрба. Дистоция плеча также увеличивает риск сдавления пуповины у ребенка и, как следствие, асфиксии при рождении и ГИЭ.Из-за рисков, связанных с дистоцией плеч, кесарево сечение — самый безопасный способ родить ребенка в этой ситуации.
Действительно, продолжительные, задержанные и затрудненные роды увеличивают многочисленные риски для ребенка. Длительное время родов травматично. Кроме того, многие состояния, связанные с длительными и затрудненными родами, повышают вероятность того, что ребенок будет подвергаться воздействию Pitocin, Cytotec, щипцов и / или вакуумных экстракторов. Все эти проблемы могут вызвать у ребенка асфиксию при рождении и мозговые кровотечения, что может вызвать гипоксическую ишемическую энцефалопатию (ГИЭ).Дистоция плеча представляет дополнительный риск паралича Эрба.
Профилактика асфиксии при рождении и ГИЭ (гипоксически-ишемическая энцефалопатия)
Профилактика асфиксии при рождении и ГИЭ (гипоксической ишемической энцефалопатии) сводится к двум основным факторам:
- Тщательное наблюдение за матерью и ребенком для выявления дистресса плода или надвигающегося дистресса
- Быстрые роды при наличии дистресса плода или надвигающегося дистресса.
Во время беременности мать и ребенок должны регулярно проходить пренатальные тесты, чтобы гарантировать здоровье плода.Если беременность связана с высоким риском, требуется более частое пренатальное тестирование, и мать должна быть направлена к специалисту по беременности и родам. Как только мать поступает в родильное отделение, к ее телу следует прикрепить кардиомонитор плода и постоянно контролировать частоту сердечных сокращений ребенка.
Кроме того, мать должна находиться под наблюдением на предмет каких-либо признаков осложнения беременности, например, затылочного канатика или отслойки плаценты. Если существуют те или иные осложнения, в большинстве случаев следует подготовиться к родоразрешению.Назначение кардиомонитора плода — предупредить медицинскую бригаду о дистрессе плода. Если ребенок испытывает недостаток кислорода в мозгу, это приведет к неутешительной записи сердечных сокращений на мониторе плода. Когда происходят неутешительные записи, медицинская бригада может попробовать реанимационные маневры, направленные на увеличение притока крови и кислорода к ребенку. Эти маневры могут включать в себя внутривенное введение жидкости или подачу кислорода матери. Однако нет гарантии, что реанимационные мероприятия уменьшат дистресс плода.Фактически, дистресс, вызванный определенными акушерскими условиями, такими как полное сдавливание пуповины или полная отслойка плаценты, не будет затронут внутриутробной реанимацией; младенцы в этих условиях должны родиться в течение нескольких минут.
При возникновении дистресса плода следует подготовиться к немедленному родоразрешению кесарева сечения во время проведения внутриутробных реанимационных мероприятий. Очень важно, чтобы квалифицированные члены медицинской бригады участвовали в родах.Для интерпретации кардиограмм плода требуется умение, и эти записи часто являются единственным признаком того, что ребенок испытывает асфиксию при родах и ГИЭ. Команда также должна быть хорошо скоординирована, чтобы подготовка и выполнение кесарева сечения были быстрыми. Задержка в проведении необходимого кесарева сечения может вызвать гипоксическую ишемическую энцефалопатию и необратимое повреждение головного мозга у ребенка.
При возникновении затяжных и затрудненных родов медицинская бригада должна очень внимательно следить за кардиомонитором плода и быть готовой к быстрому родоразрешению.Другие состояния, при которых обычно требуется быстрое кесарево сечение из-за риска асфиксии при рождении и ГИЭ (гипоксической ишемической энцефалопатии), перечислены ниже:
- Проблемы с пуповиной, такие как затылочная пуповина (пуповина, обернутая вокруг шеи ребенка), выпадение пуповины, короткая пуповина и верный узел в пуповине
- Разрыв матки
- Преэклампсия / эклампсия
- Отслойка плаценты
- Предлежание плаценты
- Ошибки при анестезии, которые могут вызвать проблемы с артериальным давлением у матери, в том числе гипотонический криз.Это может значительно снизить приток богатой кислородом крови к ребенку.
- Олигогидрамнион (малое количество околоплодных вод)
- Преждевременный разрыв плодных оболочек (PROM) / преждевременные роды
- Продолжительные и арестованные роды
- Внутричерепные кровоизлияния (мозговые кровотечения), которые могут быть вызваны травматическим родоразрешением. Щипцы и вакуумные экстракторы могут вызвать кровотечение в мозг. Иногда сильные схватки (гиперстимуляция), вызванные препаратами, стимулирующими роды (Питоцин и Цитотек), могут вызвать травму головы.Неправильное ведение головно-тазовой диспропорции (ЦФД), патологические предлежания (лицо или тазовое предлежание) и дистоция плеча также подвергают ребенка риску кровоизлияния в мозг.
- Гиперстимуляция, вызванная Pitocin и Cytotec, также может вызывать кислородную недостаточность, которая становится все более серьезной.
- Инсульт плода
- Проблемы, связанные с синдромом переношенности (макросомия, маловодие, плацентарная недостаточность и т. Д.)
Каким образом асфиксия при рождении и ГИЭ могут вызывать повреждение мозга, церебральный паралич и пожизненную инвалидность?
Когда мозг слишком долго остается без кислорода, клетки мозга повреждаются, и начинается цикл травм, который может вызвать необратимое повреждение мозга.Асфиксия при рождении и ГИЭ / гипоксическая ишемическая энцефалопатия могут вызывать следующие состояния:
Правовая помощь детям с родовыми травмами, родовой асфиксией и ГИЭ | Адвокаты в Мичиган по гипоксической ишемической энцефалопатии
Если вам нужна помощь юриста, очень важно выбрать юриста и фирму, занимающуюся исключительно случаями родовых травм. Юридические центры Reiter & Walsh ABC — это национальная юридическая фирма по родовым травмам, которая уже более 3 десятилетий помогает детям с родовыми травмами.
Если вашему ребенку был поставлен диагноз родовой травмы, такой как церебральный паралич, судорожное расстройство или гипоксическая ишемическая энцефалопатия (ГИЭ), вам могут помочь отмеченные наградами юристы по родовым травмам в юридических центрах ABC. Мы помогли детям по всей стране получить компенсацию за пожизненное лечение, терапию и безопасное будущее, и мы уделяем личное внимание каждому ребенку и семье, которые мы представляем. Наша признанная на национальном уровне фирма по травмам родовых травм имеет множество многомиллионных приговоров и расчетов, которые свидетельствуют о нашем успехе, и до тех пор, пока мы не выиграем ваше дело, нашей фирме не выплачивается никаких гонораров.Напишите или позвоните в юридические центры Reiter & Walsh ABC по телефону 888-419-2229 для бесплатной оценки дела. Отмеченные наградами юристы нашей фирмы готовы поговорить с вами круглосуточно и без выходных.
Видео: Мичиганский адвокат по асфиксии при рождении Джесси Рейтер обсуждает асфиксию при рождении и HIE
В этом видео юристы по асфиксии при рождении и HIE Джесси Рейтер и Ребекка Уолш обсуждают причины родовой травмы, асфиксии при рождении и HIE.
Источники:
- Краткое содержание: неонатальная энцефалопатия и неврологический исход, второе издание.Отчет Рабочей группы Американского колледжа акушеров и гинекологов по неонатальной энцефалопатии. Obstet Gynecol 2014; 123: 896.
- Wu YW, Backstrand KH, Zhao S, et al. Снижающийся диагноз асфиксии при рождении в Калифорнии: 1991-2000 гг. Педиатрия 2004; 114: 1584.
- Грэм Э.М., Руис К.А., Хартман А.Л. и др. Систематический обзор роли гипоксии-ишемии во время родов в возникновении неонатальной энцефалопатии. Am J Obstet Gynecol 2008; 199: 587.
- Торнберг Э, Тирингер К., Одебак А, Милсом И.Асфиксия при рождении: частота, клиническое течение и исходы среди населения Швеции. Acta Paediatr 1995; 84: 927.
- Ли А.С., Кодзуки Н., Бленкоу Н. и др. Заболеваемость и ухудшение состояния неонатальной энцефалопатии во время родов на региональном и глобальном уровнях в 2010 г. с тенденциями с 1990 г. Pediatr Res 2013; 74 Прилож. 1:50.
- Чау В., Поскитт К.Дж., Миллер СП. Передовые методы нейровизуализации доношенных новорожденных с энцефалопатией. Pediatr Neurol 2009; 40: 181.
Ссылки по теме:
Перинатальная гипоксия как фактор риска психопатологии в дальнейшей жизни: роль дофамина и нейротрофинов
Money KM, Stanwood GD (2013) Истоки развития нарушений головного мозга: роли дофамина. Front Cell Neurosci 7: 260
Статья
PubMed
PubMed Central
CAS
Google Scholar
Раттер М., Моффит Т.Э., Каспи А. (2006) Взаимодействие генов и окружающей среды и психопатология: множество разновидностей, но реальные эффекты. J Child Psychol Psychiatry 47: 226–261
Статья
PubMed
Google Scholar
Тейлор Э., Роджерс Дж. У. (2005) Обзор практикующего врача: ранние невзгоды и нарушения развития. J Child Psychol Psychiatry 46: 451–467
Статья
PubMed
Google Scholar
Кэннон Т.Д., ван Эрп Т.Г., Россо И.М. и др. (2002) Гипоксия плода и структурные аномалии головного мозга у больных шизофренией, их братьев и сестер и в контрольной группе. Arch Gen Psychiatry 59: 35–41
Статья
PubMed
Google Scholar
DeLong GR (1992) Аутизм, амнезия, гиппокамп и обучение. Neurosci Biobehav Rev 16: 63–70
Статья
PubMed
CAS
Google Scholar
Lou HC (1996) Этиология и патогенез синдрома дефицита внимания с гиперактивностью (СДВГ): значение недоношенности и перинатальной гипоксико-гемодинамической энцефалопатии. Acta Paediatr 85: 1266–1271
Статья
PubMed
CAS
Google Scholar
de Haan M, Wyatt JS, Roth S, Vargha-Khadem F, Gadian D, Mishkin M (2006) Мозг и когнитивно-поведенческое развитие после асфиксии при доношенных родах. Dev Sci 9: 350–358
Статья
PubMed
Google Scholar
Ayres-de-Campos D (2017) In: Ayres-de-Campos D (ed) Акушерские неотложные состояния: практическое руководство. Springer International Publishing, Швейцария
Google Scholar
Nelson KB, Ellenberg JH (1984) Акушерские осложнения как факторы риска церебрального паралича или судорожных расстройств. JAMA 251: 1843–1848
Статья
PubMed
CAS
Google Scholar
Колевзон А., Гросс Р., Райхенберг А. (2007) Пренатальные и перинатальные факторы риска аутизма: обзор и объединение результатов. Arch Pediatr Adolesc Med 161: 326–333
Статья
PubMed
Google Scholar
Geddes JR, Lawrie SM (1995) Акушерские осложнения и шизофрения: метаанализ. Br J Psychiatry 167: 786–793
Статья
PubMed
CAS
Google Scholar
Geddes JR, Verdoux H, Takei N et al (1999) Шизофрения и осложнения беременности и родов: метаанализ индивидуальных данных пациентов. Schizophr Bull 25: 413–423
Статья
PubMed
CAS
Google Scholar
Verdoux H, Geddes JR, Takei N et al (1997) Акушерские осложнения и возраст начала шизофрении: международный совместный метаанализ данных отдельных пациентов. Am J Psychiatry 154: 1220–1227
Статья
PubMed
CAS
Google Scholar
Dahl A, Boerdahl P (1993) Акушерские осложнения как фактор риска последующего развития расстройств личности. J Pers Dis 7: 22–27
Статья
Google Scholar
Латимер К., Уилсон П., Кемп Дж. И др. (2012) Расстройства деструктивного поведения: систематический обзор факторов риска дородового и раннего возраста, связанных с окружающей средой. Child Care Health Dev 38: 611–628
Статья
PubMed
CAS
Google Scholar
Кэннон М., Джонс П.Б., Мюррей Р.М. (2002) Акушерские осложнения и шизофрения: исторический и метааналитический обзор. Am J Psychiatry 159: 1080–1092
Статья
PubMed
Google Scholar
Dalman C, Allebeck P, Cullberg J, Grunewald C, Koster M (1999) Акушерские осложнения и риск шизофрении: продольное исследование национальной когорты новорожденных. Arch Gen Psychiatry 56: 234–240
Статья
PubMed
CAS
Google Scholar
Done DJ, Johnstone EC, Frith CD, Golding J, Shepherd PM, Crow TJ (1991) Осложнения беременности и родов в связи с психозом во взрослой жизни: данные британского исследования перинатальной смертности.BMJ 302: 1576–1580
Статья
PubMed
PubMed Central
CAS
Google Scholar
Россо И.М., Кэннон Т.Д., Хуттунен Т., Хуттунен М.О., Лоннквист Дж., Гасперони Т.Л. (2000) Факторы акушерского риска ранней шизофрении в финской когорте новорожденных. Am J Psychiatry 157: 801–807
Статья
PubMed
CAS
Google Scholar
Buka SL, Tsuang MT, Lipsitt LP (1993) Осложнения беременности / родов и психиатрический диагноз.Перспективное исследование. Arch Gen Psychiatry 50: 151–156
Статья
PubMed
CAS
Google Scholar
Кэннон Т.Д., Россо И.М., Холлистер Дж.М., Бирден С.Е., Санчес Л.Е., Хэдли Т. (2000) Проспективное когортное исследование генетических и перинатальных влияний на этиологию шизофрении. Schizophr Bull 26: 351–366
Статья
PubMed
CAS
Google Scholar
Zammit S, Odd D, Horwood J et al (2009) Изучение того, связаны ли неблагоприятные пренатальные и перинатальные события с неклиническими психотическими симптомами в возрасте 12 лет в когорте рожденных alspac. Psychol Med 39: 1457–1467
Статья
PubMed
CAS
Google Scholar
Hanssen M, Bak M, Bijl R, Vollebergh W, van Os J (2005) Частота и исход субклинических психотических переживаний в общей популяции.Br J Clin Psychol 44: 181–191
Статья
PubMed
Google Scholar
Заммит С., Кунали Д., Кэннон М. и др. (2013) Психотические переживания и психотические расстройства в возрасте 18 лет в связи с психотическими переживаниями в возрасте 12 лет в продольном популяционном когортном исследовании. Am J Psychiatry 170: 742–750
Статья
PubMed
Google Scholar
Nosarti C, Reichenberg A, Murray RM et al (2012) Преждевременные роды и психические расстройства в молодом возрасте.Arch Gen Psychiatry 69: E1 – E8
Статья
PubMed
Google Scholar
Гарденер Х., Шпигельман Д., Бука С.Л. (2011) Перинатальные и неонатальные факторы риска аутизма: всесторонний метаанализ. Педиатрия 128: 344–355
Статья.
PubMed
PubMed Central
Google Scholar
Бен Амор Л., Гризенко Н., Шварц Г. и др. (2005) Перинатальные осложнения у детей с синдромом дефицита внимания и гиперактивности и их здоровых братьев и сестер.J Psychiatry Neurosci 30: 120–126
PubMed
PubMed Central
Google Scholar
Getahun D, Rhoads GG, Demissie K et al (2012) Внутриутробное воздействие ишемически-гипоксических состояний и синдрома дефицита внимания / гиперактивности. Педиатрия 131: e53 – e61
Статья
PubMed
Google Scholar
Сейдман Л.Дж., Валера Е.М., Макрис Н. (2005) Структурная визуализация мозга при синдроме дефицита внимания / гиперактивности.Biol Psychiatry 57: 1263–1272
Статья
PubMed
Google Scholar
Howes OD, Kapur S (2009) Допаминовая гипотеза шизофрении: версия iii — последний общий путь. Schizophr Bull 35: 549–562
Статья
PubMed
PubMed Central
Google Scholar
Howes OD, Williams M, Ibrahim K et al (2013) Функция дофамина среднего мозга при шизофрении и депрессии: исследование посмертной и позитронно-эмиссионной томографии.Мозг 136: 3242–3251
Статья
PubMed
PubMed Central
Google Scholar
Pagida MA, Konstantinidou AE, Tsekoura E, Mangoura D, Patsouris E, Panayotacopoulou MT (2013) Уязвимость мезэнцефальных дофаминергических нейронов новорожденного человека к пролонгированной перинатальной гипоксии: исследование иммуногистопсии иммуногистопсии. материал. J Neuropathol Exp Neurol 72: 337–350
Статья
PubMed
CAS
Google Scholar
Panayotacopoulou MT, Swaab DF (1993) Развитие тирозингидроксилазо-иммунореактивных нейронов в паравентрикулярном и супраоптическом ядрах человека. Brain Res Dev Brain Res 72: 145–150
Статья
PubMed
CAS
Google Scholar
Bjelke B, Andersson K, Ogren SO, Bolme P (1991) Асфиктическое поражение: пролиферация тирозингидроксилазо-иммунореактивных нервных клеток в черной субстанции крысы и функциональные изменения в нейротрансмиссии дофамина.Brain Res 543: 1–9
Статья
PubMed
CAS
Google Scholar
Brake WG, Boksa P, Gratton A (1997) Влияние перинатальной аноксии на острую двигательную реакцию на повторное введение амфетамина у взрослых крыс. Психофармакология 133: 389–395
Статья
PubMed
CAS
Google Scholar
Burke RE, Macaya A, DeVivo D, Kenyon N, Janec EM (1992) Гипоксически-ишемическое или эксайтотоксическое повреждение полосатого тела у новорожденных приводит к уменьшению количества нейронов черной субстанции у взрослых.Neuroscience 50: 559–569
Статья
PubMed
CAS
Google Scholar
Chen Y, Herrera-Marschitz M, Bjelke B, Blum M, Gross J, Andersson K (1997) Изменения, вызванные перинатальной асфиксией, в количестве тирозингидроксилазных иммунореактивных клеток головного мозга крысы: эффекты лечения никотином. Neurosci Lett 221: 77–80
Статья
PubMed
CAS
Google Scholar
Бокса П., Эль-Ходор Б.Ф. (2003) Инсульт при рождении взаимодействует со стрессом во взрослом возрасте, изменяя дофаминергическую функцию в моделях на животных: возможные последствия для шизофрении и других расстройств. Neurosci Biobehav Rev 27: 91–101
Статья
PubMed
CAS
Google Scholar
Pagida MA, Konstantinidou AE, Korelidou A et al (2016) Влияние перинатального гипоксического / ишемического повреждения на экспрессию тирозингидроксилазы в голубом пятне новорожденного человека.Dev Neurosci 38: 41–53
Статья
PubMed
CAS
Google Scholar
Ganou V, Pagida MA, Konstantinidou AE et al (2010) Повышенная экспрессия тирозингидроксилазы в супраоптическом ядре новорожденного человека в условиях гипоксии: потенциальный нейропатологический маркер длительной перинатальной гипоксии. J Neuropathol Exp Neurol 69: 1008–1016
Статья
PubMed
CAS
Google Scholar
Pagida MA, Konstantinidou AE, Malidelis YI et al (2013) Нейросекреторные нейроны человека в условиях перинатальной гипоксии: количественное иммуногистохимическое исследование супраоптического ядра в материале аутопсии. J Нейроэндокринол 25: 1255–1263
Статья
PubMed
CAS
Google Scholar
Pagida MA, Konstantinidou AE, Tsekoura E, Patsouris E, Panayotacopoulou MT (2013) Иммуногистохимическая демонстрация урокортина 1 в ядре эдингера-вестфала у новорожденного человека: совместная локализация с помощью острой гипоксиназы тирозина.Neurosci Lett 554: 47–52
Статья
PubMed
CAS
Google Scholar
Дэвис Дж. Н. (1976) Гидроксилирование тирозина в мозге: изменение сродства к кислороду in vivo путем иммобилизации или электрошока у крысы. J Neurochem 27: 211–215
Статья
PubMed
CAS
Google Scholar
Feinsilver SH, Wong R, Raybin DM (1987) Адаптация синтеза нейромедиаторов к хронической гипоксии в культуре клеток.Biochim Biophys Acta 928: 56–62
Статья
PubMed
CAS
Google Scholar
Czyzyk-Krzeska MF, Beresh JE (1996) Характеристика сайта связывания индуцируемого гипоксией белка в богатом пиримидином тракте в 3′-нетранслируемой области тирозингидроксилазы мРНК. J Biol Chem 271: 3293–3299
Статья
PubMed
CAS
Google Scholar
Paulding WR, Schnell PO, Bauer AL et al (2002) Регулирование экспрессии генов нейромедиаторов во время адаптации к гипоксии в чувствительных к кислороду нейроэндокринных клетках. Microsc Res Tech 59: 178–187
Статья
PubMed
CAS
Google Scholar
Schmidt-Kastner R, van Os J, Esquivel G, Steinbusch HW, Rutten BP (2012) Анализ окружающей среды генов, связанных с шизофренией: гипоксия и сосудистые факторы как взаимодействующие элементы в модели развития нервной системы.Mol Psychiatry 17: 1194–1205
Статья
PubMed
CAS
Google Scholar
Fallet-Bianco C (2005) Диагностика и датирование гипоксически-ишемической энцефалопатии 20-й Европейский конгресс патологов. Франция, Париж, стр. 127–132
Google Scholar
Rorke-Adams L, Larroche J, de Vries L (2007) Повреждение мозга плода и новорожденного. В: Gilbert-Barness E (ed) Патология Поттера плода, младенца и ребенка.Мосби-Эльзевьер, Филадельфия, стр. 2027–2053
Google Scholar
Squier W (2004) Поражения серого вещества. В: Golden J, Harding B (eds) Патология и генетика, невропатология развития. ISN Neuropathology Press, Базель, стр 171–175
Google Scholar
Романос М., Вайзе Д., Шлиссер М. и др. (2010) Структурная аномалия черной субстанции у детей с синдромом дефицита внимания и гиперактивности.J Psychiatry Neurosci 35: 55–58
Статья
PubMed
PubMed Central
Google Scholar
Bogerts B, Hantsch J, Herzer M (1983) Морфометрическое исследование дофамин-содержащих групп клеток в среднем мозге нормальных людей, пациентов с паркинсонизмом и шизофреников. Biol Psychiatry 18: 951–969
PubMed
CAS
Google Scholar
Какабелос Р. (2017) Болезнь Паркинсона: от патогенеза к фармакогеномике.Int J Mol Sci 18: 551–578
Статья
PubMed Central
CAS
Google Scholar
Burke RE, Kent J, Kenyon N, Karanas A (1991) Одностороннее гипоксически-ишемическое повреждение у новорожденных крыс приводит к стойкому увеличению плотности окрашивания иммунопероксидазой тирозингидроксилазы полосатого тела. Brain Res Dev Brain Res 58: 171–179
Статья
PubMed
CAS
Google Scholar
Mittal VA, Ellman LM, Cannon TD (2008) Взаимодействие генов и окружающей среды и ковариация при шизофрении: роль акушерских осложнений. Schizophr Bull 34: 1083–1094
Статья
PubMed
PubMed Central
Google Scholar
Miyamoto S, LaMantia AS, Duncan GE, Sullivan P, Gilmore JH, Lieberman JA (2003) Последние достижения в нейробиологии шизофрении. Mol Interv 3: 27–39
Статья
PubMed
Google Scholar
Ван Эрп Т.Г., Салех П.А., Россо И.М. и др. (2002) Вклад генетического риска и гипоксии плода в объем гиппокампа у пациентов с шизофренией или шизоаффективным расстройством, их здоровых братьев и сестер и здоровых неродственных добровольцев. Am J Psychiatry 159: 1514–1520
Статья
PubMed
Google Scholar
Curatolo P, Paloscia C, D’Agati E, Moavero R, Pasini A (2009) Нейробиология синдрома дефицита внимания / гиперактивности.Eur J Paediatr Neurol 13: 299–304
Статья
PubMed
Google Scholar
Tripp G, Wickens JR (2009) Neurobiology of ADHD. Нейрофармакология 57: 579–589
Статья
PubMed
CAS
Google Scholar
Prince J (2008) Дисфункция катехоламинов при синдроме дефицита внимания / гиперактивности: обновленная информация. J Clin Psychopharmacol 28 (Приложение 2): 39–45
Статья
CAS
Google Scholar
Барлоу Б.К., Кори-Слехта Д.А., Ричфилд Е.К., Тиручелвам М. (2007) Гестационная среда и болезнь Паркинсона: доказательства нейродегенеративного происхождения нейродегенеративного расстройства. Reprod Toxicol 23: 457–470
Статья
PubMed
CAS
PubMed Central
Google Scholar
Reinebrant HE, Wixey JA, Buller KM (2013) Гипоксия-ишемия новорожденных нарушает нисходящие нервные входы в ядра дорсального шва. Неврология 248C: 427–435
Статья
CAS
Google Scholar
Buller KM, Wixey JA, Pathipati P et al (2008) Избирательная потеря катехоламиновых нейронов ствола головного мозга после гипоксии-ишемии у неполовозрелого детеныша крысы. Pediatr Res 63: 364–369
Статья
PubMed
CAS
Google Scholar
Homberg JR, Molteni R, Calabrese F, Riva MA (2014) Дуэт серотонин-BDNF: последствия для развития уязвимости к психопатологии. Neurosci Biobehav Rev 43: 35–47
Статья
PubMed
CAS
Google Scholar
Kuppers E, Beyer C (2001) Дофамин регулирует экспрессию нейротрофического фактора мозга (BDNF) в культивируемых эмбриональных клетках полосатого тела мыши. Нейрорепорт 12: 1175–1179
Статья
PubMed
CAS
Google Scholar
Autry AE, Monteggia LM (2012) Нейротрофический фактор головного мозга и нейропсихиатрические расстройства. Pharmacol Rev 64: 238–258
Статья
PubMed
PubMed Central
CAS
Google Scholar
Cannon TD, Yolken R, Buka S, Torrey EF (2008) Снижение нейротрофического ответа на гипоксию при рождении в этиологии шизофрении. Biol Psychiatry 64: 797–802
Статья
PubMed
PubMed Central
CAS
Google Scholar
Кейси Б.Дж., Глатт С.Е., Тоттенхэм Н. и др. (2009) Нейротрофический фактор мозга как модельная система для изучения взаимодействия гена с окружающей средой в процессе развития. Неврология 164: 108–120
Статья
PubMed
PubMed Central
CAS
Google Scholar
Shoval G, Weizman A (2005) Возможная роль нейротрофинов в патогенезе и терапии шизофрении. Eur Neuropsychopharmacol 15: 319–329
Статья
PubMed
CAS
Google Scholar
Husson I, Rangon CM, Lelievre V et al (2005) BDNF-индуцированная нейрозащита белого вещества и стадийно-зависимая выживаемость нейронов после неонатальной эксайтотоксической нагрузки. Cereb Cortex 15: 250–261
Статья
PubMed
Google Scholar
Хенниган А., О’Каллаган Р.М., Келли А.М. (2007) Нейротрофины и их рецепторы: роли в пластичности, нейродегенерации и нейропротекции. Biochem Soc Trans 35: 424–427
Статья
PubMed
CAS
Google Scholar
Hetman M, Xia Z (2000) Сигнальные пути, опосредующие антиапоптотическое действие нейротрофинов. Acta Neurobiol Exp (Wars) 60: 531–545
CAS
Google Scholar
Karege F, Schwald M, Cisse M (2002) Постнатальный профиль развития нейротрофического фактора головного мозга в головном мозге и тромбоцитах крыс. Neurosci Lett 328: 261–264
Статья
PubMed
CAS
Google Scholar
Цирулли Ф., Франсия Н., Берри А., Алоэ Л., Аллева Е., Суоми С.Дж. (2009) Стресс в раннем возрасте как фактор риска для психического здоровья: роль нейротрофинов от грызунов до нечеловеческих приматов. Neurosci Biobehav Rev 33: 573–585
Статья
PubMed
CAS
Google Scholar
Cirulli F, Berry A, Alleva E (2003) Ранний разрыв отношений между матерью и младенцем: влияние на пластичность мозга и последствия для психопатологии. Neurosci Biobehav Rev 27: 73–82
Статья
PubMed
CAS
Google Scholar
Рао Р., Машберн С.Б., Мао Дж., Вадхва Н., Смит Г.М., Десаи Н.С. (2009) Нейротрофический фактор головного мозга у младенцев <32 недель гестационного возраста: корреляция с антенатальными факторами и послеродовыми исходами.Pediatr Res 65: 548–552
Статья
PubMed
PubMed Central
CAS
Google Scholar
Чаутхай Н.С., Самперс Дж., Десаи Н., Смит Г.М. (2003) Изменения уровней нейротрофинов в пуповинной крови у младенцев с разным гестационным возрастом и клиническими состояниями. Pediatr Res 53: 965–969
Статья
PubMed
CAS
Google Scholar
Маламитси-Пухнер А., Эконому Э., Ригопулу О., Буцику Т. (2004) Перинатальные изменения нейротрофического фактора головного мозга у недоношенных и доношенных новорожденных.Early Hum Dev 76: 17–22
Статья
PubMed
CAS
Google Scholar
Николау К.Э., Маламитси-Пухнер А., Буцику Т. и др. (2006) Различные паттерны изменений нейротрофинов в перинатальном периоде. Ann N Y Acad Sci 1092: 426–433
Статья
PubMed
CAS
Google Scholar
Бернд П. (2008) Роль нейротрофинов на раннем этапе развития.Gene Expr 14: 241–250
Статья
PubMed
Google Scholar
Kawamura K, Kawamura N, Kumazawa Y, Kumagai J, Fujimoto T, Tanaka T (2011) Передача сигналов нейротрофического фактора мозга / тирозинкиназы b из мозга регулирует рост трофобластов человека в модели внематочной беременности in vivo на животных. Эндокринология 152: 1090–1100
Статья
PubMed
CAS
Google Scholar
Mayeur S, Lukaszewski MA, Breton C, Storme L, Vieau D, Lesage J (2011) Регулируют ли нейротрофины фетоплацентарное развитие? Med Hypotheses 76: 726–728
Статья
PubMed
CAS
Google Scholar
Korhonen L, Riikonen R, Nawa H, Lindholm D (1998) Нейротрофический фактор головного мозга повышен в спинномозговой жидкости детей, страдающих асфиксией. Neurosci Lett 240: 151–154
Статья
PubMed
CAS
Google Scholar
Миллер Ф.Д., Каплан Д.Р. (2001) Пути передачи сигналов нейротрофина, регулирующие апоптоз нейронов. Cell Mol Life Sci 58: 1045–1053
Статья
PubMed
CAS
Google Scholar
Eide MG, Moster D, Irgens LM, Reichborn-Kjennerud T, Stoltenberg C, Skjaerven R, Susser E, Abel K (2013) Степень ограничения роста плода, связанного с риском шизофрении в национальной когорте. Psychol Med 43: 2057–2066
Статья
PubMed
CAS
Google Scholar
Van Lieshout RJ, Voruganti LP (2008) Сахарный диабет во время беременности и повышенный риск шизофрении у потомства: обзор доказательств и предполагаемых механизмов. J Psychiatry Neurosci 33: 395–404
PubMed
PubMed Central
Google Scholar
Coupe B, Dutriez-Casteloot I, Breton C et al (2009) Перинатальное недоедание изменяет пролиферацию клеток и уровни нейротрофических факторов мозга в критические временные окна для развития гипоталамуса и гиппокампа у самцов крыс.J Neuroendocrinol 21: 40–48
Статья
PubMed
CAS
Google Scholar
Ниномия М., Нумакава Т., Адачи Н. и др. (2010) Кортикальные нейроны крыс с задержкой внутриутробного развития демонстрируют более низкий ответ на нейротрофин BDNF. Neurosci Lett 476: 104–109
Статья
PubMed
CAS
Google Scholar
Маламитси-Пухнер А., Николау К.Э., Эконому Е. и др. (2007) Ограничение внутриутробного развития и уровни циркулирующих нейротрофинов в срок.Early Hum Dev 83: 465–469
Статья
PubMed
CAS
Google Scholar
Mayeur S, Silhol M, Moitrot E et al (2010) Плацентарная сигнальная система BDNF / TRKB модулируется нарушениями роста плода у крысы и человека. Плацента 31: 785–791
Статья
PubMed
CAS
Google Scholar
Бриана Д.Д., Папаставру М., Буцику М., Мармаринос А., Гурджотис Д., Маламитси-Пухнер А. (2017) Дифференциальная экспрессия нейротрофинов пуповинной крови при гестационном диабете: влияние аномалий роста плода.J Matern Fetal Neonatal Med: 1–6
Boersma GJ, Lee RS, Cordner ZA et al (2014) Пренатальный стресс снижает экспрессию BDNF и увеличивает метилирование экзона BDNF iv у крыс. Эпигенетика 9: 437–447
Статья
PubMed
Google Scholar
Kundakovic M, Gudsnuk K, Herbstman JB, Tang D, Perera FP, Champagne FA (2015) Метилирование ДНК BDNF как биомаркер невзгод раннего возраста. Proc Natl Acad Sci U S A 112: 6807–6813
Статья
PubMed
CAS
Google Scholar
Дефицит кислорода у плода | Де-Мойн, адвокат по травмам
Когда плод не получает достаточного количества кислорода в матке во время роста, это состояние называется внутриутробной гипоксией.Непосредственно перед или во время родов и родов кислородное голодание плода называется гипоксией плода или гипоксией во время родов. Все три термина относятся к состоянию, при котором ткани ребенка получают недостаточное количество кислорода, что может привести к серьезным осложнениям, включая гипоксические травмы головного мозга. Неонатальная асфиксия используется для описания ребенка сразу после рождения, который не начинает дышать или дыхание которого не обеспечивает организм достаточным количеством кислорода. Если мозг лишен значительного количества кислорода в любое время во время беременности или после рождения, необратимое повреждение головного мозга (внутрижелудочковое кровоизлияние, перивентрикулярная лейкомаляция и т. Д.) и / или другие осложнения.
Симптомы
До рождения можно заподозрить гипоксию плода, если есть признаки дистресса плода. Во время родов и родоразрешения будущая мать будет иметь внешние и, возможно, внутренние мониторы, прикрепленные к ней и / или ее ребенку, чтобы отслеживать ее сокращения (силу и частоту), а также частоту сердечных сокращений ее ребенка. Информация, поступающая с этих мониторов, выводится на полосу для мониторинга состояния плода, которую акушер, акушерская медсестра или акушерская сестра могут использовать, чтобы увидеть, как ребенок реагирует на каждое сокращение и на роды в целом.Низкая частота сердечных сокращений плода (брадикардия) или необычное замедление частоты сердечных сокращений ребенка (позднее замедление) могут быть признаком дистресс-синдрома плода. Кроме того, необычный характер вариабельности сердечного ритма плода может указывать на травму головного мозга или надвигающееся повреждение мозга или центральной нервной системы ребенка. Если есть признаки дистресс-синдрома плода и роды достаточно прогрессируют, врач или медсестра может взять образец pH с головы ребенка, чтобы проверить, не наблюдается ли кислородная недостаточность.
Ребенок, лишенный кислорода до рождения, может испытывать затруднения при дыхании после рождения, иметь слишком много кислоты в жидкостях организма, проявляться поражением или расстройствами мозга или иметь поврежденные органы. Если кислородное голодание происходило во время родов, ребенок может быть синим при рождении, у него не будет звуков дыхания, не будет крика, плохой мышечный тонус или низкая частота сердечных сокращений. Оценка ребенка по шкале APGAR может быть низкой, а анализ газов артериальной крови может показывать низкий pH (т.е. <7,1) или повышенный базовый избыток. Забор крови из пуповины может быть взят для документирования pH ребенка и избытка основания во время рождения.Низкий pH может означать, что ребенок страдает метаболическим ацидозом (низким содержанием кислорода) в результате негативных последствий родов.
После рождения у ребенка (чаще недоношенного) может развиться респираторный дистресс-синдром (РДС). Сразу после рождения ребенок может быть розовым, с хорошим плачем, хорошим мышечным тонусом и нормальной частотой сердечных сокращений. Однако в течение нескольких минут после рождения у ребенка может развиться RDS с признаками хрюканья, удушья или затрудненного дыхания. У недоношенных детей это может произойти из-за того, что легкие плода еще не созрели.В этом случае ребенку может потребоваться дополнительный кислород через маску или может потребоваться интубация эндотрахеальной трубки для искусственной вентиляции легких, чтобы помочь ребенку дышать. Восстановление доставки кислорода называется «реанимацией» ребенка. Если реанимация не происходит, у ребенка может развиться респираторный ацидоз, о чем свидетельствует высокий уровень CO2 в крови ребенка. Этот респираторный ацидоз увеличивает риск того, что у ребенка может развиться мозговое кровотечение, также известное как внутрижелудочковое кровоизлияние (ВЖК).ВЖК может привести к сопутствующим проблемам, таким как церебральный паралич. Если реанимация не обеспечивает ребенка достаточным количеством кислорода, у ребенка также может развиться метаболический ацидоз, о чем свидетельствует низкий уровень pH в крови ребенка. Низкий уровень кислорода может вызвать аноксическое или гипоксическое повреждение головного мозга ребенка, ведущее к перивентрикулярной лейкомаляции (ПВЛ) и церебральному параличу (ЦП).
Независимо от того, происходит ли кислородная недостаточность внутриутробно или после рождения, необходимо своевременное вмешательство и процедуры реанимации, чтобы гарантировать, что ребенок восстановит адекватное снабжение кислородом, чтобы предотвратить гипоксию, повреждение мозга или смерть.
Некоторые факторы риска гипоксии плода в период гестации включают
- Плод, крупный для гестационного периода / дети с высокой массой тела при рождении (макросомный)
- В матке слишком много околоплодных вод
- Таз матери слишком мал для родов (головно-тазовая диспропорция)
- Экскреция мекония
- Многоплодие (двойня, тройня и т. Д.)
- Проблемы с беременностью — отслойка плаценты, предлежание плаценты, разрыв матки, обильное кровотечение
- Осложнения, связанные с несовместимостью матери и плода по резус-фактору
Младенцы подвергаются большему риску асфиксии во время схваток и родов, когда мать находится под воздействием каких-либо лекарств, особенно анестетиков или седативных средств, потому что до момента рождения мать делится с плодом любыми веществами, которые находятся в ее крови. поток.Например, обезболивающие, вводимые женщине во время родов, могут оказывать респираторное воздействие на ребенка при рождении. Таким образом, медицинские работники должны знать, что такие лекарства могут вызвать угнетение дыхания у ребенка и недостаток кислорода, если их не исправить.
У недоношенных младенцев может не быть полностью развитой дыхательной системы, которая может обеспечить их организм достаточным количеством кислорода. Таким образом, если преждевременные роды неизбежны, медицинские работники должны знать о необходимости назначения стероидов (например, бетаметазона) для созревания легких плода.Кроме того, медицинский персонал должен знать о возможной потребности в сурфактанте у недоношенных детей.
Затяжные или проблемные роды могут подвергнуть плод риску таких состояний, как выпадение или повреждение пуповины, что лишает плод адекватного снабжения кислородом. Затяжные роды также могут израсходовать запасы кислорода у ребенка, что делает его более восприимчивым к гипоксии на последнем этапе родов.
Роды, в которых используются акушерские инструменты, такие как вакуум-экстрактор или щипцы, имеют более высокий риск травмирования младенца и могут привести к условиям, ограничивающим приток кислорода к мозгу и другим органам.У доношенных плодов больше предрасположенности к выделению мекония до рождения и существует риск аспирации липкого вещества, которое может блокировать дыхательные пути. У младенцев также может развиться пневмония после контакта с организмом Strep-B, который некоторые женщины переносят в родовых путях. Любое другое состояние, которое приводит к рождению ребенка с «тяжелым респираторным дистресс-синдромом», может привести к гипоксии, если дыхание не восстанавливается достаточно быстро.
Поскольку естественные роды и родоразрешение помогают плоду изгнать жидкость, которая была в легких на протяжении всей беременности, у детей, родившихся после кесарева сечения, могут возникнуть трудности с адаптацией к дыханию вне матки.
Осложнения
Дефицит кислорода может привести к гипоксии, когда ткани тела нарушены из-за недостатка кислорода. Все органы тела подвержены повреждению из-за недостаточного снабжения кислородом, но когда мозг получает повреждение (гипоксическая ишемическая энцефалопатия, также известная как ГИЭ), могут возникнуть серьезные последствия. Повреждение от недостатка кислорода может привести к параличам, умственной отсталости, повреждению нервов, порокам сердца, нарушениям свертываемости крови, коме и даже смерти. Документально подтверждено, что 23% смертей новорожденных вызваны асфиксией или кислородным голоданием.
Профилактика
Многие причины пренатальной кислородной недостаточности практически невозможно обнаружить, а доступные методы лечения некоторых выявляемых причин не доказали свою эффективность. Во время беременности, если есть какие-либо аномалии органов, которые обнаруживаются на УЗИ или сонограмме, можно провести дополнительные тесты, чтобы изучить частоту сердечных сокращений плода и общее состояние здоровья ребенка. Женщинам с семейным анамнезом врожденных дефектов, диабетикам или женщинам, подвергавшимся воздействию токсинов (в том числе лекарств и медикаментов), может быть рекомендовано пройти тестирование на вероятность наличия у их плода определенных хромосомных или генетических дефектов.Правильное лечение материнских заболеваний и заболеваний во время беременности может снизить опасность неблагоприятных воздействий на растущий плод. Адекватный дородовой уход способствует снижению риска осложнений для здоровья как матери, так и ребенка.
Лечение
До 20% младенцев, рожденных с тяжелой церебральной гипоксией, не выживают, а от 20 до 25% становятся инвалидами. Для младенцев, рожденных с тяжелой гипоксической ишемической энцефалопатией (ГИЭ), новые методы лечения, включающие охлаждающую терапию или гипотермию головы или тела, оказались успешными в снижении стойких неврологических повреждений и предотвращении смерти от недостатка кислорода в головном мозге у ряда пациентов.Диагностика и лечение основных причин кислородного голодания способствуют предотвращению дальнейшего повреждения. После родов тщательный медицинский осмотр и тщательное наблюдение в первые несколько дней жизни могут выявить любые проблемы, требующие немедленного лечения для предотвращения серьезных осложнений. Правильное просвещение родителей относительно предупреждающих признаков гипоксии, таких как цианоз, и точное описание симптомов, а также подробный семейный анамнез и записи о пренатальном уходе могут привести к правильной диагностике причины гипоксии у младенца.
Если вашему ребенку был поставлен диагноз церебральный паралич, гипоксическая ишемическая энцефалопатия, перивентрикулярная лейкомаляция или внутрижелудочковое кровоизлияние, вам следует собрать свои медицинские записи, а также медицинские записи вашего ребенка и передать их на рассмотрение юристу, имеющему опыт работы со случаями врачебной халатности. гипоксические травмы или кислородное голодание.
Гипоксия плода и структурные аномалии мозга у больных шизофренией, их братьев и сестер и контрольной группы | Врожденные пороки | JAMA Psychiatry
Фон
Уменьшение количества серого вещества в корковом веществе и увеличение спинномозговой жидкости (ЦСЖ) являются надежными коррелятами шизофрении, но их связь с акушерскими и другими этиологическими факторами риска еще предстоит установить.
Методы
Структурированные диагностические интервью, записи акушерского стационара и магнитно-резонансная томография головного мозга были получены у 64 пациентов с шизофренией или шизоаффективностью (репрезентативны для всех таких пробандов в когорте рождения Хельсинки, Финляндия), а также у 51 их непсихотических полных братьев и сестер и 54 демографически сходные контрольные группы без семейных историй психозов.
Результаты
Гипоксия плода предсказывала уменьшение серого вещества и увеличение спинномозговой жидкости с двух сторон по всей коре у пациентов (размер эффекта серого вещества, −0.От 31 до -0,56; Размер эффекта CSF от 0,25 до 0,47) и братьев и сестер (размер эффекта серого вещества от 0,33 до 0,47; размер эффекта CSF от 0,17 до 0,33), наиболее сильно в височной доле. Величина эффекта была в 2–3 раза выше среди случаев, рожденных маленькими для их гестационного возраста. Гипоксия также достоверно коррелировала с увеличением желудочков, но только у пациентов (величина эффекта 0,31). Напротив, гипоксия плода не была связана ни с белым веществом у пациентов и братьев и сестер, ни с каким-либо типом ткани в любом регионе в контрольной группе.Ассоциации не зависели от членства в семье, общего объема мозга, возраста, пола, злоупотребления психоактивными веществами и пренатальной инфекции.
Выводы
Гипоксия плода связана с более выраженными структурными аномалиями головного мозга у больных шизофренией и их братьев и сестер, не являющихся шизофрениками, чем среди контрольной группы с низким генетическим риском шизофрении. Этот образец результатов указывает на учет взаимодействия генов и окружающей среды в патогенезе нервного развития расстройства.
СТРУКТУРНЫЕ НАРУШЕНИЯ МОЗГА — надежные корреляты шизофрении, но их причины окончательно не установлены. 1 -3 Нейромоторный и когнитивный дефициты у детей дошизофрении 4 -6 и смещение кортикальных ламинарных нейронов у больных шизофренией при вскрытии 7 -10 предполагают, что по крайней мере некоторые из анатомических изменений имеют нервное развитие по происхождению. 11 Генетические влияния на шизофрению значительны, 12 , но способ наследования сложен. Он включает в себя по крайней мере несколько генов 13 и определенные нервно-разрушающие воздействия окружающей среды, такие как акушерские осложнения (ОК). 14 -27 Из многих типов ОК, обнаруженных для прогнозирования шизофрении, гипоксия плода показала наиболее сильную связь, составляя большую долю риска, чем воздействие инфекций во время беременности, задержки роста плода и других акушерских факторов. 27 Поскольку ни одно исследование с использованием объективных записей о рождении не показало, что гипоксические ОК чаще встречаются у родственников первой степени родства больных шизофренией, чем в общей популяции, 17 -24 эти осложнения, по-видимому, не являются следствием генетического предрасположенность к шизофрении.Также маловероятно, что эти ранние влияния сами по себе вызывают шизофрению, потому что более 90% людей, которые испытывают гипоксию плода, даже в ее тяжелой форме, не заболевают шизофренией. 17 , 18,25 , 26 Гипоксические ОК должны, таким образом, действовать аддитивно или интерактивно с генетическими факторами, влияя на предрасположенность к заболеванию. 27
В предыдущем исследовании компьютерной томографии мы нашли доказательства, подтверждающие модель взаимодействия генов и окружающей среды в отношении вклада гипоксии плода в подкорковые аномалии у больных шизофренией. 28 Соотношение желудочков и головного мозга увеличивалось в связи с наличием в анамнезе ОКК, связанных с гипоксией, среди потомков родителей-шизофреников, но не среди потомков контрольной группы, тогда как соотношение борозды и головного мозга варьировалось в зависимости от степени генетической нагрузки шизофрении, но не в акушерстве. факторы изучены. Эти данные свидетельствуют о том, что генетический фактор шизофрении может сделать мозг плода особенно восприимчивым к повреждению перивентрикулярной ткани после гипоксии. Интерпретируемость этих данных ограничена, однако, ограниченным локализующим значением анатомических показателей на основе спинномозговой жидкости (CSF) 2 и сомнительной обобщаемостью результатов, полученных от потомков матерей с необычно тяжелыми формами шизофрении. 29 Кроме того, исследование с помощью магнитно-резонансной томографии (МРТ) монозиготных близнецов, дискордантных по шизофрении, обнаружило большие желудочки и меньшие объемы височных долей у пораженных по сравнению с непораженными близнецами, различия, которые должны отражать негенетические влияния 30 ; Эти внутрипарные различия в размерах желудочков и гиппокампа связаны с более высокой частотой ОК у пораженных близнецов. 31
Ранее мы сообщали о различиях в региональной морфологии головного мозга, оцененной с помощью МРТ, у пациентов с шизофренией, их братьев и сестер, не являющихся шизофрениками, и у контрольной группы с низким генетическим риском шизофрении. 32 У пациентов и их братьев и сестер было уменьшение серого вещества и увеличение ликвора борозды в лобных и височных областях с обеих сторон, но не в задних областях. Пациенты, но не братья и сестры, также показали увеличение желудочков и уменьшение общего белого вещества по сравнению с контрольной группой. В рамках этого исследования мы также собрали оригинальные акушерские истории болезни субъектов. Было обнаружено, что наличие в анамнезе ОК, связанных с гипоксией, но не внутриутробных инфекций или задержки роста плода, позволяет прогнозировать повышенный риск ранней шизофрении. 18 В этом анализе мы использовали одни и те же образцы, чтобы определить, была ли гипоксия плода по-разному связана с увеличением желудочков и уменьшением объема височных долей у пациентов и братьев и сестер с повышенным риском шизофрении по сравнению с контрольной группой с низким генетическим риском.
Участников было отобрано из общей популяции людей, родившихся в Хельсинки, Финляндия, в 1955 году, и всех их полных братьев и сестер (N = 7840 и N = 12 796, соответственно) с использованием ранее описанных методов. 12 , 32 Национальные компьютеризированные базы данных были использованы для скрининга когорты на предмет наличия в анамнезе психических расстройств, требующих лечения, и потенциальные пробанды были случайным образом выбраны из этого общего пула. Право на участие было ограничено пробандами с пожизненным диагнозом шизофрения или шизоаффективного расстройства при прямом собеседовании DSM-III-R 33 . Около 75% опрошенных дали информированное согласие и соответствовали критериям включения. Исследуемые пробанды были эквивалентны остальной популяции пробандов с точки зрения года рождения, размера нуклеарной семьи, пола, возраста при первом поступлении в стационар, истории психического расстройства и нетрудоспособности, но в исследуемой группе в среднем было 1 балл.На 5 госпитализаций больше, чем в неисследованной группе. 32 Была предпринята попытка привлечь по крайней мере одного не шизофренического брата для каждого исследуемого пробанда, но это было возможно только в 62 из 80 случаев. Кроме того, 56 субъектов контрольной группы, не страдающих шизофренией (из 28 пар братьев и сестер), были выбраны из одной и той же когорты рождения после исключения тех, кто в личном или семейном анамнезе проходил психиатрическое лечение. Субъекты контроля были похожи на пробандов и их братьев и сестер по демографическим переменным. Все субъекты были опрошены с использованием структурированного клинического интервью для DSM-III-R расстройств 34 , проводимого психологами и социальными психиатрическими работниками, прошедшими обширную предварительную подготовку; братья и сестры и члены контрольной группы также были опрошены по пунктам кластера А из экзамена на расстройство личности. 35 Диагностическая надежность была превосходной (κ = 0,94 ± 0,02), 36 , и окончательные диагнозы были поставлены на основе консенсуса между 3 независимыми оценщиками.
Отсутствие записей акушерского стационара (n = 21) и / или технические проблемы с МРТ (n = 7) исключили 27 субъектов из анализа. Таблица 1 показывает, что пациенты, братья и сестры и контрольные группы были сбалансированы по злоупотреблению психоактивными веществами и основным демографическим и акушерским переменным.
Исследователь, слепой к диагностике и результатам визуализации, использовал стандартную форму для кодирования информации из исходных записей женской консультации и родовспомогательной больницы о здоровье матери, мониторинге плода, пренатальных и перинатальных осложнениях и состояниях новорожденных.Акушерские переменные, использованные в анализе, были небольшими для статуса гестационного возраста (т. Е. Масса тела при рождении на уровне или ниже 10-го процентиля для данного гестационного возраста), любой материнской инфекции (краснуха, грипп и т. Д.) Во время беременности и гипоксии плода. Гипоксия плода оценивалась как присутствующая, если субъект был обозначен синим цветом при рождении или новорожденном или имел 2 или более осложнения, которые были существенно связаны с асфиксией при рождении или неонатальной асфиксии в общей выборке. Осложнения включали завязывание пуповины или туго обернутую вокруг шеи, инфаркт плаценты, кровотечение в третьем триместре, преэклампсию, анемию во время беременности, анорексию во время беременности, отклонения частоты сердечных сокращений / ритма плода и тазовое предлежание.Недоношенность была удалена из определения гипоксии, ранее использовавшегося 18 , чтобы дать возможность оценить эффекты гипоксии как функцию статуса развития. Поскольку почти все субъекты, родившиеся преждевременно (т. Е. ≥2 недель), были маленькими для своего гестационного возраста, и наоборот, эти две категории были объединены.
Изображения были получены с использованием стандартной последовательности двойных эхо-сигналов с толщиной среза 5 мм и сегментированы на серое вещество, белое вещество и CSF с использованием адаптивного 3-мерного байесовского алгоритма 38 , ранее утвержденного для этой цели. 39 Эти объемы были разделены по полушариям и областям с использованием оперативно определенных границ для лобных и височных долей. 40 Кроме того, «задняя» область была определена как вся ткань, за исключением лобной и височной долей. Трассировки проводились вслепую в отношении диагноза и истории рождений, и межэкспертная надежность была превосходной (внутриклассовые корреляции> 0,93). Дополнительные сведения, относящиеся к процедурам получения и анализа МРТ, представлены в другом месте. 32
Данные были проанализированы с использованием общей линейно-смешанной модели с повторными измерениями. Мы скорректировали зависимость (т. Е. Корреляцию) между несколькими наблюдениями из одной семьи и одного и того же человека, рассматривая семью и человека, вложенного в семью, как случайные переменные и соответствующим образом скорректировав условия ошибки модели. Измерения серого вещества, белого вещества, борозды ЦСЖ и ЦСЖ желудочков анализировались отдельно, при этом полушарие и, где это уместно, область (лобная, височная, задняя) рассматривались как внутренние переменные с повторными измерениями.Мы проверили гипотезу о том, что гипоксия плода сильнее связана с морфологией мозга при наличии генетической предрасположенности к шизофрении, моделируя взаимодействие группы риска и гипоксии плода, как в целом, так и во взаимодействии с полушарием и регионом, в качестве предиктора фиксированного эффекта. Чтобы определить, зависят ли эти эффекты от недоношенных / малых для статуса гестационного возраста, мы также смоделировали взаимодействие группы риска × гипоксия плода × мало для статуса гестационного возраста, как в целом, так и во взаимодействии с полушарием и регионом.Всякий раз, когда один из этих терминов значительно предсказывал объем мозга, проводился контрастный анализ для сравнения субъектов с гипоксией в анамнезе и без нее в каждой группе риска после коллапса по несущественным измерениям внутри субъекта. Этот подход поддерживал процент ошибок типа I на уровне 0,05, оценивая вклад предиктора в зависимую меру только в том случае, если его влияние было значительным на многомерном уровне. Инфекция матери во время беременности была включена в качестве предиктора для контроля возможного искажения связи между гипоксическими ОК и объемами мозга.Было слишком мало субъектов с историей материнской инфекции для значимого теста ее потенциального взаимодействия с группой риска. Кроме того, при анализе учитывались общий объем мозга, возраст на момент обследования, пол и анамнез расстройства, связанного с употреблением психоактивных веществ, поскольку эти индивидуальные различия могут объяснять некоторую вариабельность в региональных объемах мозга. Для корректировки межобластных различий в размере интересующей области объемы регионарной ткани выражали в виде процентных соотношений общих региональных объемов (например, соотношение серого вещества во фронтальной области = [объем серого вещества во фронтальной области / общий объем во фронтальной части] × 100).
Смешанная модель, анализ соотношений серого вещества в регионах и полушариях, белого вещества и спинномозговой жидкости в головном мозге на основе смешанной модели показал, что гипоксия плода является значимым предиктором серого вещества (F 1,111 = 14,6, P <0,001) и общая борозда ЦСЖ (F 1,144 = 8,3, P = 0,005). Анализы также показали, что гипоксия плода значительно взаимодействует с группой риска при прогнозировании общего серого вещества (F 2,95 = 6, P =.003), с незначительными тенденциями в этом направлении для общей борозды CSF (F 2,125 = 2,7, P = 0,07) и общей желудочковой CSF (F 2135 = 2,7, P = 0,07). Как для серого вещества (F 10,785 = 6,8, P <0,001), так и для спинномозговой жидкости (F 10,785 = 7,0, P <0,001), термин взаимодействия группа риска × гипоксия плода значительно варьировался как функция региона, но не функция полушария или региона внутри полушария.Как показано в Таблице 2, несмотря на то, что было отмечено значительное сокращение серого вещества, связанного с гипоксией плода, во всех регионах среди пациентов и братьев и сестер, величина этой связи была наибольшей в височной доле для обеих групп. Та же картина наблюдалась в отношении увеличения регионарной борозды у пациентов, в то время как у братьев и сестер гипоксия была в значительной степени связана с увеличением борозды только в височной доле. Гипоксия плода также была связана со значительным увеличением ЦСЖ желудочков, но только у пациентов.Напротив, гипоксия плода не была существенно связана с белым веществом ни в одной группе и не была существенно связана с каким-либо типом ткани в любой области для контроля.
Недоношенность / малый размер для гестационного возраста
Наблюдалось основное влияние статуса малого для гестационного возраста на серое вещество (F 1,125 = 4.8, P = 0,03) и борозды CSF (F 1,152 = 3,8, P = 0,05). Взаимодействие группы риска и гипоксии плода варьировалось незначительно в зависимости от малого для гестационного возраста статуса серого вещества (F 5,98 = 1,9, P = 0,10), со значительной тенденцией в этом направлении для бороздчатого СХУ. (F 5,128 = 2,5, P = 0,04), изображенные на рисунках 1 и 2 соответственно. Связь гипоксии плода с уменьшением серого вещества и увеличением борозды у пациентов и их братьев и сестер была значительно выше (т. Е. Величина эффекта была в 2-3 раза больше) среди тех, кто родился недоношенным и / или маленьким для своего гестационного возраста.Среди субъектов, родившихся доношенными и / или нормальными для их гестационного возраста, гипоксия плода была связана со значительным уменьшением серого вещества только у пациенток. Напротив, малый для гестационного возраста статус не был связан с серым веществом или бороздой спинномозговой жидкости в отсутствие гипоксии, и не было значимой связи между гипоксией плода и серым веществом или бороздой спинномозговой жидкости в контрольной группе, независимо от статуса развития при рождении.
Инфекция оказала значительное общее основное воздействие на серое вещество (F 1,108 = 7.8, P = 0,006) и борозды CSF (F 1,137 = 6,2, P = 0,014), но не на белом веществе или спинномозговой жидкости желудочков. Субъекты, у которых в анамнезе была материнская инфекция во время беременности, имели более низкое соотношение серого вещества — и более высокое отношение спинномозговой жидкости к мозгу, чем те, у кого этого не было (среднее ± SEM, 54,3 ± 0,7 против 56,3 ± 0,3 для серого вещества; 10,5 ± 1,0 против 8,0 ± 0,4 для серого вещества; бороздчатый ликвор).
Общий объем мозга достоверно предсказал серое вещество (F 1,149 = 19.1, P <0,001), белого вещества (F 1,132 = 29,1, P <0,001) и ЦСЖ желудочков (F 1,128 = 4,8, P = 0,03). Возраст при сканировании и злоупотребление психоактивными веществами значительно предсказывали объем серого вещества (F 1,138 = 6,7, P = 0,01; F 1,100 = 3,6, P = 0,04, соответственно). После учета общего объема мозга секс не давал достоверного предсказания каких-либо объемов.
Главный вывод этого исследования состоит в том, что гипоксия плода в анамнезе связана с увеличением структурных аномалий мозга у пациентов с шизофренией и их братьев и сестер, не являющихся шизофрениками, но не среди контрольной группы с низким генетическим риском заболевания.В следующих параграфах мы рассмотрим основные конкурирующие объяснения наших выводов с указанием их возможных последствий.
Во-первых, связь между гипоксией плода и измененной нейроанатомией может быть объяснена другими ОК, которые как увеличивают риск шизофрении, так и нарушают работу мозга с помощью механизмов, отличных от кислородной недостаточности или в дополнение к ней. Однако мы рассмотрели 2 наиболее известных таких кандидата, пренатальную инфекцию и задержку роста плода, и обнаружили, что ни один из них не коррелировал с гипоксией плода или шизофренией у взрослых.Более того, контроль этих двух факторов статистически не изменил значимости или величины ассоциаций между гипоксией плода и морфологией мозга у пациентов или братьев и сестер. Тем не менее, можно ожидать, что некоторые случаи задержки роста плода связаны с такими состояниями, как плацентарная недостаточность, которые вызывают легкую, но хроническую гипоксию плода. 41 В соответствии с этой точкой зрения, ассоциации гипоксии плода с морфологией мозга были значительно увеличены среди пациентов и братьев и сестер, родившихся маленькими для их гестационного возраста.Однако, поскольку задержка роста плода не предсказывала значительных изменений морфологии мозга в отсутствие гипоксии, задержка роста сама по себе не конкурирует с гипоксией как механизмом, лежащим в основе этих ассоциаций.
Можно также утверждать, что наши результаты предполагают влияние, отличное от гипоксии, потому что не наблюдались некоторые из хорошо описанных макроскопических последствий для мозга, таких как перивентрикулярное повреждение белого вещества. Однако нервные последствия гипоксии многочисленны и зависят от тяжести и времени поражения.На клеточном уровне они различаются по степени тяжести от изменений в росте нейритов до гибели нейрональных клеток. 42 Только в последнем случае можно ожидать потери как серого, так и белого вещества. В первом случае незрелые нейроны могут пережить гипоксическое воздействие, но все же иметь скомпрометированную выработку синаптических взаимосвязей. 42 Исследования на плодных овцах показали, что гипоксия, вторичная по отношению к хронической плацентарной недостаточности, связана с уменьшением толщины кортикального слоя и повышением плотности кортикальных нейронов без какой-либо наблюдаемой потери нейронов или повреждения белого вещества. 43 Это уменьшение объема нейропиля должно проявляться как уменьшение объема серого, но не белого вещества на макроскопическом уровне. Таким образом, картина морфологических изменений, связанных с гипоксией в этом исследовании, совместима с моделью хронической гипоксии плода на животных. Эта интерпретация также подтверждается тем фактом, что более 80% субъектов в группе гипоксии плода имели положительные маркеры как пренатальной, так и родовой асфиксии.
Другая возможность состоит в том, что эффекты гипоксии могут быть смешаны с общими генетическими факторами или факторами окружающей среды, которые увеличивают вероятность гипоксических осложнений у пациентов и их незатронутых братьев и сестер.Однако у братьев и сестер не было более высоких показателей ОК, связанных с гипоксией, чем в контрольной группе, 18 , что указывает на отсутствие ковариации между этими ОК и статусом генетического риска. Хотя ковариацию между гипоксией и общим влиянием окружающей среды нельзя полностью исключить, исследования близнецов и усыновлений показали, что общая среда играет незначительную роль в общей этиологии шизофрении. 12 , 44 Более того, трудно представить себе систематическое влияние окружающей среды, которое проявлялось бы в большей восприимчивости к гипоксически-ишемическому повреждению головного мозга и которое разделялось бы несогласованными с шизофренией братьями и сестрами, но не демографически подобранной контрольной группой.Наиболее вероятными из таких кандидатов являются пренатальная вирусная инфекция и задержка роста плода, которые не были более распространены у пациентов и их братьев и сестер и не являлись причиной значительных эффектов гипоксии.
Мы также можем исключить возможность того, что наши выводы являются следствием отбора нерепрезентативной выборки пробандов. В этом исследовании использовался метод случайной выборки на основе популяций, который привел к отличному соответствию между изученными и неизученными пробандами по основным демографическим и клиническим переменным.Более того, поскольку группы братьев и сестер и контрольные группы были хорошо сопоставимы по наличию серьезных психических расстройств, наши результаты не связаны с преобладанием психических заболеваний, не связанных с шизофренией, среди братьев и сестер.
Таким образом, кажется, что ОК, ассоциированные с гипоксией, каким-то образом связаны с патогенезом шизофрении нервной системы. В контексте расстройства с полигенным наследованием 45 ОК могут действовать либо аддитивно, либо интерактивно с генетическими факторами, повышая риск шизофрении с непрерывной ответственностью. 27 Аддитивная модель предсказывает, что гипоксия должна иметь эквивалентную степень влияния на постоянные маркеры предрасположенности к заболеванию, независимо от степени генетического фона расстройства. Модель взаимодействия предсказывает, что гипоксия плода должна иметь дифференциальную связь с постоянными маркерами предрасположенности к заболеванию у лиц с повышенным генетическим риском шизофрении по сравнению с теми, кто находится в низком генетическом риске. Наше открытие о том, что гипоксия плода связана с увеличением признаков аномалий мозга как у пациентов, так и у их братьев и сестер, но не среди контрольной группы с низким уровнем риска, таким образом, согласуется с моделью взаимодействия генов.Эта модель также подтверждается нашим более ранним исследованием, которое показало, что гипоксические осложнения предсказывают повышенный риск шизофрении и большее увеличение желудочков у потомков родителей-шизофреников, но не у потомков родителей, не являющихся шизофрениками. 20 , 28 Увеличение кортикальной борозды не зависело от акушерского анамнеза среди лиц с генетическим риском шизофрении в датском исследовании, 28 , как это было в настоящем исследовании, что, скорее всего, отражает большее снижение сигнала в корковая поверхность (из-за артефактов частичного объема), связанная с компьютерной томографией, по сравнению с МРТ.
Модель взаимодействия генов с окружающей средой делает 2 дополнительных прогноза, которые можно проверить на этой выборке: (1) гипоксия плода должна встречаться чаще среди пациентов с шизофренией, чем среди их братьев и сестер, и (2) связь между гипоксией плода и индикаторами постоянной ответственности должна отличаться от пациентов по сравнению с их братьями и сестрами. Хотя в этом исследовании частота гипоксии плода не различалась по группам риска, в предыдущем отчете по этой выборке было обнаружено, что количество ОК, связанных с гипоксией, было повышено среди случаев с ранним возрастом в начале, но не среди случаев с более поздним началом или среди братьев и сестер одного из них. группа. 18 Более того, вероятность раннего начала шизофрении увеличивалась в 2,9 раза на гипоксический ОК в семьях. 18 Поскольку в этом отчете рассматривалась взаимосвязь ОК и морфологии мозга, а не диагноз, и из-за ограниченного размера выборки, случаи с ранним и более поздним началом были сведены вместе в анализах. Тот факт, что у большинства пациентов с гипоксией плода в анамнезе были случаи раннего начала, повышает вероятность того, что воздействие гипоксии смешано с другими факторами, которые определяют возраст начала.Однако связь между гипоксией плода и морфологией головного мозга оставалась значимой после того, как данные пациентов были повторно проанализированы с возрастом на момент начала заболевания в качестве дополнительной ковариаты (F 1,54 = 7,8, P = 0,007 для серого вещества; F 1 , 54 = 4,8, P = 0,03 для спинномозговой жидкости желудочков и F 1,54 = 7,9, P = 0,007 для спинномозговой жидкости желудочков).
В соответствии со вторым предсказанием, эффект гипоксии был значительно больше среди пациентов, чем у братьев и сестер, для серого вещества обоих типов (F 6,535 = 6.53, P <0,001) и борозды CSF (F 6,535 = 6,20, P <0,001) и присутствовали только среди пациентов с желудочковой CSF (Таблица 2). Таким образом, хотя здоровые братья и сестры проявляют некоторую чувствительность к способствующим шизофрении эффектам гипоксии плода, эта чувствительность отличается от наблюдаемой у пациентов как количественно (по кортикальным измерениям), так и качественно (по поводу увеличения желудочков).
Эти данные добавляют к растущим свидетельствам того, что по крайней мере некоторые из аномалий головного мозга у больных шизофренией имеют нервное происхождение. 11 То, что увеличение желудочков и уменьшение объема серого вещества коры коррелировали с неблагоприятным состоянием при рождении, ясно указывает на раннее происхождение этих аномалий, хотя никоим образом не исключает участия более поздних процессов развития нервной системы 46 или нейродегенеративных процессов 47 . Также кажется вероятным, что гены, предрасполагающие к шизофрении, могут сделать мозг плода особенно уязвимым для гипоксических ОК. Это открытие стимулирует поиск генов, повышающих уязвимость мозга к гипоксическому / ишемическому повреждению нейронов.
Это исследование имеет несколько ограничений. Мы использовали T2-взвешенные изображения с большой толщиной среза (5 мм), которые более подвержены частичным объемным артефактам, чем T1-взвешенные изображения с более высоким разрешением. Такие эффекты усиливаются при увеличении борозды и, следовательно, могут влиять на диагностический статус. Однако, поскольку основное влияние артефакта частичного объема заключается в снижении отношения сигнал / шум, тем самым уменьшая способность обнаруживать истинные ассоциации, наличие такого взаимодействия в этих данных, скорее всего, привело бы к недооценке эффекта. размеры в группах пациентов и братьев и сестер.В этом исследовании также использовались относительно крупные анатомические подразделения, из-за чего неясно, отражает ли связь между гипоксией и потерей серого вещества в задней области уменьшение объема подкорковых структур, затылочно-теменной коры или и того, и другого. Влияние на заднее серое вещество представляется вероятным, поскольку примерно 80% объема заднего отдела приходится на затылочно-теменную кору. Связь гипоксии с подкорковыми аномалиями также представляется вероятной, учитывая ее корреляцию с увеличением желудочков, которое при шизофрении связано с уменьшением перивентрикулярного серого вещества. 48 , 49
Поскольку большинство субъектов с гипоксией плода в анамнезе имели положительные маркеры как пренатальной, так и перинатальной гипоксии, мы не смогли проверить, возникает ли гипоксия в разное время в развитии (ожидается, что это приведет к разным паттернам регионарной травмы головного мозга 50 , 51 ) по-разному относится к структурным аномалиям головного мозга при шизофрении. Кроме того, наше определение воздействия гипоксии ограничивалось осложнениями, которые были зарегистрированы в записях о рождении в финской системе здравоохранения в течение 1950-х годов.Хотя эти записи имеют высокое качество и содержат акушерские измерения, которые явно превосходят данные, полученные при ретроспективном опросе матери, более прямые количественные методы анализа оксигенации крови плода 52 , 53 позволили бы более чувствительно проверить наши гипотезы.
Принята к публикации 6 июня 2001 г.
Это исследование было поддержано грантом Mh58207 Национального института психического здоровья, Бетесда, штат Мэриленд.
Мы благодарим Уллу Мустонен, MSW, и Лийзу Варонен, PhD, за их вклад в набор и оценку субъектов; Антти Тансканен, MS, за его вклад в поиск в реестре и создание базы данных; Мэри О’Брайен, доктор философии, за ее вклад в диагностические процедуры и оценку надежности; и Ракель Гур, доктор медицинских наук, Брюс Турецкий, доктор медицинских наук, Мишель Ян, доктор философии, и другие исследователи из Клинического исследовательского центра психического здоровья факультета психиатрии Пенсильванского университета, Филадельфия (грант Mh53880), за их вклад в методы визуализации. и процедуры анализа, использованные в этом исследовании.
Автор для переписки и оттиски: Тайрон Д. Кэннон, доктор философии, факультет психологии, Калифорнийский университет, Лос-Анджелес, 1285 Франц Холл, Лос-Анджелес, Калифорния
(электронная почта: [email protected]).
1. пушка
Т.Д. Нарушения структуры и функции мозга при шизофрении: значение для этиологии и патофизиологии. Ann Med. 1996; 28533-539Google ScholarCrossref 2. Buchanan
RWCarpenter
WT Нейроанатомия шизофрении. Schizophr Bull. 1997; 23367-372Google ScholarCrossref 3.Pfefferbaum
AMarsh
L Структурная визуализация мозга при шизофрении. Clin Neurosci. 1995; 3105-111Google Scholar 4. Россо
IMBearden
CEHollister
JMGasperoni
TLSanchez
LEHadley
TCannon
TD Детская нейромоторная дисфункция у пациентов с шизофренией и их здоровых братьев и сестер: проспективное когортное исследование. Schizophr Bull. 2000; 26367-378Google ScholarCrossref 5.Пушка
TDBearden
CEHollister
JMRosso
IMSanchez
LEHadley
T Когнитивное функционирование в детстве у пациентов с шизофренией и их здоровых братьев и сестер: проспективное когортное исследование. Schizophr Bull. 2000; 26379-393Google ScholarCrossref 6. Walker
EF Модерированные в развитии проявления невропатологии, лежащей в основе шизофрении. Schizophr Bull. 1994; 20453-480Google ScholarCrossref 7. Акбарян
SBunney
МЫ
JrPotkin
SGWigal
SBHagman
JOSandman
CAJones
Э.Г. Изменение распределения никотинамид-адениндинуклеотид-фосфат-диафоразных клеток в лобной доле у шизофреников свидетельствует о нарушении коркового развития. Arch Gen Psychiatry. 1993; 50169-177Google ScholarCrossref 8. Акбарян.
SVinuela
AKim
JJPotkin
SGBunney
МЫ
JrJones
Э.Г. Искаженное распределение нейронов никотинамид-аденин-динуклеотид-фосфат-диафоразы в височной доле у шизофреников свидетельствует об аномальном развитии коры головного мозга. Arch Gen Psychiatry. 1993; 50178-187Google ScholarCrossref 9. Арнольд
SEHyman
BTVan Hoesen
GWDamasio
А.Р. Некоторые цитоархитектурные аномалии энторинальной коры при шизофрении. Arch Gen Psychiatry. 1991; 48625-632Google ScholarCrossref 10.Benes
FMMcSparren
JBird
EDSan Giovanni
JPVincent
Дефицит SL в малых интернейронах префронтальной и поясной коры шизофренических и шизоаффективных пациентов. Arch Gen Psychiatry. 1991; 48996-1001Google ScholarCrossref 11. Пушка
Т.Д. Влияние нервного развития на генезис и эпигенез шизофрении: обзор. Appl Prev Psychol. 1998; 747-62Google ScholarCrossref 12. Пушка
TDKaprio
JLönnqvist
JHuttunen
МОКоскенвуо
M Генетическая эпидемиология шизофрении в финской когорте близнецов: исследование на основе популяционного моделирования. Arch Gen Psychiatry. 1998; 5567-74Google ScholarCrossref 14.Jones
PBRantakallio
PHartikainen
Алисоханни
MSipila
P Шизофрения как отдаленный исход беременности, родов и перинатальных осложнений: 28-летнее наблюдение в когорте общего населения Северной Финляндии, родившейся в 1966 году. Am J Psychiatry. 1998; 155355-364Google Scholar15.Eagles
JMGibson
И.Бремнер
MHClunie
Фебмайер
KPSmith
NC Акушерские осложнения у DSM-III шизофреников и их братьев и сестер. Ланцет. 1990; 3351139–1141Google ScholarCrossref 16.Kinney
DKLevy
DLЮргелун-Тодд
DAMedoff
DLaJonchere
CMRadford-Paregol
M Сезон родов и акушерские осложнения у шизофреников. J Psychiatr Res. 1994; 28499-509Google ScholarCrossref 17.Cannon
TDRosso
IMHollister
JMBearden
CESanchez
LEHadley
T Проспективное когортное исследование генетических и перинатальных влияний на этиологию шизофрении. Schizophr Bull. 2000; 26351-366Google ScholarCrossref 18. Россо
IMCannon
TDHuttunen
MOHuttunen
TLönnqvist
JGasperoni
TL Факторы акушерского риска ранней шизофрении в финской когорте новорожденных. Am J Psychiatry. 2000; 157801-807Google ScholarCrossref 19. Гюнтер-Гента
FBovet
PHohlfeld
P Акушерские осложнения и шизофрения: исследование случай-контроль. Br J Психиатрия. 1994; 164165-170Google ScholarCrossref 20. Мирдал
GKMednick
SASchulsinger
FFuchs
F Перинатальные осложнения у детей матерей-шизофреников. Acta Psychiatr Scand. 1974; 50553-568Google ScholarCrossref 21.Marcus
JAuerback
JWilkinson
LBurack
CM Младенцы в группе риска шизофрении: Иерусалимское исследование развития младенцев. Arch Gen Psychiatry. 1981; 38703-713Google ScholarCrossref 22. Рыба
BMarcus
JHans
SLAuerbach
JGPerdue
S Младенцы из группы риска шизофрении: последствия генетического нейроинтегративного дефекта. Arch Gen Psychiatry. 1992; 49221-235Google ScholarCrossref 23.Hanson
DRGottesman
IIХестон
LL Некоторые возможные детские индикаторы взрослой шизофрении, полученные от детей шизофреников. Br J Психиатрия. 1976; 129142-154Google ScholarCrossref 24.Rieder
ROBroman
Ш.Розенталь
D Потомство шизофреников, II: перинатальные факторы и IQ. Arch Gen Psychiatry. 1977; 34789-799Google ScholarCrossref 25.Buka
SLTsuang
MTLipsitt
LP Осложнения беременности / родов и психиатрический диагноз: проспективное исследование. Arch Gen Psychiatry. 1993; 50151-156Google ScholarCrossref 26.Done
DJJohnstone
ECFrith
CDGolding
JShepherd
PMCrow
TJ Осложнения беременности и родов в связи с психозом во взрослой жизни: данные британского исследования перинатальной смертности. BMJ. 1991; 3021576-1580Google ScholarCrossref 27.Cannon
Т.Д. О природе и механизмах акушерских влияний при шизофрении: обзор и обобщение эпидемиологических исследований. Int Rev Psychiatry. 1997; 9387-397Google ScholarCrossref 28.Cannon
TDMednick
SAParnas
JSchulsinger
FPraestholm
JVestergaard
А аномалии развития мозга у потомков матерей-шизофреников, I: вклад генетических и перинатальных факторов. Arch Gen Psychiatry. 1993; 50551-564Google ScholarCrossref 29.Parnas
JCannon
Т. Д. Якобсен
BSchulsinger
HSchulsinger
FMednick
SA Lifetime DSM-III-R Диагностические результаты у потомков матерей с шизофренией: результаты Копенгагенского исследования высокого риска. Arch Gen Psychiatry. 1993; 50707-714Google ScholarCrossref 30.Suddath
RLChristison
GWTorrey
Е.Ф.Касанова
М.Ф.Вайнбергер
DR Анатомические аномалии в головном мозге монозиготных близнецов, несовместимые с шизофренией. N Engl J Med. 1990; 322789-794Google ScholarCrossref 31.McNeil
Т.Ф. Кантор-Граэ
EWeinberger
DR Связь акушерских осложнений и различий в размерах структур мозга в парах монозиготных близнецов, дискордантных по шизофрении. Am J Psychiatry. 2000; 157203-212Google ScholarCrossref 32.Cannon
ТДван Эрп
TGMHuttunen
MLönnqvist
JSalonen
OValanne
LPoutanen
VPStandertskjöld-Nordenstam
CGGur
Рейан
M Региональное распределение серого вещества, белого вещества и спинномозговой жидкости у больных шизофренией, их братьев и сестер и в контрольной группе. Arch Gen Psychiatry. 1998; 551084-1091Google ScholarCrossref 33.
Американская психиатрическая ассоциация, Диагностическое и статистическое руководство по психическим расстройствам , 3-е изд. Вашингтон, округ Колумбия, Американская психиатрическая ассоциация, 1987;
34.
Спитцер
Р.Л.Уильямс
JBGibbon
M Руководство по структурированному клиническому интервью для DSM-III-R (SCID) . Вашингтон, округ Колумбия, Американская психиатрическая ассоциация, 1987;
35.
Loranger
AWSussman
VLOldham
Ю.М.Русаков
LM Обследование расстройства личности.Структурированное интервью для диагностики расстройств личности DSM-III-R. Уайт-Плейнс, Корнеллский медицинский колледж штата Нью-Йорк 1985;
37. Рахаула
U Количественная сила социальных слоев финского общества. Sosiaalinen-Aikakauskirja. 1970; 63347-362Google Scholar 38.Yan
MXKarp
JS Адаптивный байесовский подход к трехмерной МРТ сегментации мозга. Bizais
YBarillot
CDi Paola
Reds Обработка информации в медицинской визуализации New York, NY Kluwer Academic Publishers, 1995; 201–213, Google Scholar39.Goldszal
ADavatzikos
CPham
ДЛЯН
MXBryan
Р.Н.Ресник
SM Система обработки изображений для качественного и количественного объемного анализа изображений головного мозга. J Comput Assist Tomogr. 1998; 22827-837Google ScholarCrossref 40.Turetsky
BTCowell
ПЭГур
RCGrossman
РИШтасель
DLGur
RR Объемы головного мозга лобных и височных долей при шизофрении: взаимосвязь с симптоматикой и клиническим подтипом. Arch Gen Psychiatry. 1995; 521061-1070Google ScholarCrossref 41. Richardson
BSBocking
А.Д. Метаболическая адаптация и адаптация кровообращения к хронической гипоксии у плода. Comp Biochem Physiol A Mol Integr Physiol. 1998; 119717-723Google ScholarCrossref 43.Rees
SMallard
CBreen
SStringer
MCock
MHarding
R Повреждение головного мозга плода после длительной гипоксемии и плацентарной недостаточности: обзор. Comp Biochem Physiol A Mol Integr Physiol. 1998; 119653-660Google ScholarCrossref 44.Kendler
К.С.Грюнберг
AMKinney
DK Независимые диагнозы усыновленных и родственников согласно определению в DSM-III в провинциальных и национальных выборках датского исследования шизофрении в области усыновления. Arch Gen Psychiatry. 1994; 51456-468Google ScholarCrossref 45.
Gottesman
IIShields
J Шизофрения: эпигенетическая головоломка . Кембридж, Англия Издательство Кембриджского университета 1982;
46.Кешаван
MSAnderson
SPettegrew
JW Является ли шизофрения результатом чрезмерного сокращения синапсов в префронтальной коре? пересмотр гипотезы Файнберга. J Psychiatr Res. 1994; 28239-265Google ScholarCrossref 47.Gur
RECowell
Птурецкий
BIGallacher
FCannon
TDBilker
WGur
RC Последующее исследование шизофрении с помощью магнитно-резонансной томографии: взаимосвязь нейроанатомических изменений с клиническими и нейроповеденческими показателями. Arch Gen Psychiatry. 1998; 55145-152Google ScholarCrossref 48.Brown
RColter
NCorsellis
Янкроу
TJFrith
CDJagoe
RJohnstone
ECMarsh
L Посмертные доказательства структурных изменений мозга при шизофрении: различия в массе мозга, площади височных рогов и парагиппокампальной извилине по сравнению с аффективным расстройством. Arch Gen Psychiatry. 1986; 4336-42Google ScholarCrossref 49.Lesch
ABogerts
B Промежуточный мозг при шизофрении: данные об уменьшении толщины перивентрикулярного серого вещества. Eur Arch Psychiatry Neurol Sci. 1984; 234212-219Google ScholarCrossref 50.Barkovich
AJHallam
D Нейровизуализация при перинатальном гипоксически-ишемическом повреждении. Ment Retard Dev Disabil Res Rev. 1997; 328-41Google ScholarCrossref 51.Volpe
JJ Гипоксически-ишемическая энцефалопатия: невропатология и патогенез. Неврология новорожденных 3rd Philadelphia, PA WB Saunders1995; 279-312Google Scholar52.Low
JA. Роль газов крови и измерения кислотно-щелочного баланса в диагностике асфиксии плода во время родов. Am J Obstet Gynecol. 1988; 15
-1240Google ScholarCrossref 53.Buescher
UHertwig
KWolf
CDudenhausen
JW. Эритропоэтин в околоплодных водах как маркер хронической гипоксии плода. Int J Gynaecol Obstet. 1998; 60257-263Google ScholarCrossref
Внутриутробная гипоксия: биоинформатика болезней: Novus Biologicals
Разместите свое изображение, связанное с болезнями, чтобы оно было размещено!
Социальные сети
Разместите свою учетную запись Twitter, посвященную внутриутробной гипоксии, чтобы ее разместили!
Блоги
Разместите свой блог о внутриутробной гипоксии, чтобы его разместили! |
События
| Разместите ваше мероприятие по внутриутробной гипоксии, чтобы быть популярным! |
Видео
Отправьте свое видео о внутриутробной гипоксии, чтобы его разместили!
Благотворительные организации
Отправьте свою благотворительную организацию по теме «Внутриутробная гипоксия», чтобы ее разместили!
Внутриутробная гипоксия или ИГ возникает в результате того, что плод лишен доступа к кислороду непосредственно перед, во время или сразу после родов.ИГ может быть вызвано множеством причин, таких как выпадение пуповины, окклюзия пуповины, инфаркт плаценты и курение матери. Ограничение внутриутробного развития может вызвать или быть результатом гипоксии. Асфиксия при родах может возникнуть из-за продолжительных родов, тазовых предлежаний. Кислородная недостаточность — наиболее частая причина перинатального повреждения головного мозга. Внутриутробная гипоксия может вызвать гипоксическую ишемическую энцефалопатию, которая представляет собой повреждение клеток головного и спинного мозга. Это повреждение также может вызвать повышенный риск синдрома внезапной детской смерти.Недостаток кислорода у плода может привести к таким расстройствам, как эпилепсия, СДВГ, расстройства пищевого поведения и церебральный паралич, которые будут влиять на ребенка на протяжении всей его жизни.
Инструмент для биоинформатики внутриутробной гипоксии
Laverne — это удобный инструмент биоинформатики, помогающий облегчить научное исследование родственных генов, болезней и путей на основе совместного цитирования. Узнайте больше о внутриутробной гипоксии ниже!
Для получения дополнительной информации о том, как использовать Laverne, прочтите Руководство.
Реагенты Top Research
У нас есть 2281 продукт для исследования внутриутробной гипоксии, который можно применять для вестерн-блоттинга, проточной цитометрии, иммуноцитохимии / иммунофлуоресценции, иммуногистохимии из нашего каталога антител и наборов для ELISA.
| 3 Обзоры 80 Публикации | Добавить в корзину |
NBP2-52631
| 1 Публикация | Добавить в корзину |
| 6 Публикаций | Добавить в корзину |
| 26 Обзоры 519 Публикации | Добавить в корзину |
| 26 Обзоры 478 Публикации | Добавить в корзину |
NBP2-75520
Кролик Моноклональный
Виды Человек
Приложения WB, ICC / IF, IHC
NB100-858
Коза Поликлональная
Виды Человек, мышь, крыса
Приложения WB, Flow, ICC / IF
| 1 Обзор 13 Публикации | Добавить в корзину |
NB300-605
Кролик Поликлональный
Виды Человек, Мышь, Крыса
Применения WB, Flow, IB
| 3 Обзоры 57 Публикации | Добавить в корзину |
Виды Человек, мышь, крыса
| 1 Обзор 63 Публикации | Добавить в корзину |
| 6 Обзоров 40 Публикаций | Добавить в корзину |
NBP1-78444
Кролик Поликлональный
Виды Человек, Мышь, Крыса
Приложения WB, Simple Western, ICC / IF
| 2 Обзоры 11 Публикации | Добавить в корзину |
NBP2-47415
Кролик Поликлональный
Виды Человек
Приложения WB, ICC / IF, IHC
| 4 Обзоры 83 Публикации | Добавить в корзину |
| 3 Публикации | Добавить в корзину |
NBP2-45267
Мышь Моноклональная
Виды Человек
Приложения WB, Flow, ICC / IF
NBP1-84318
Кролик Поликлональный
Виды Человек
Приложения WB, IHC, IHC-P
| 35 Обзоров 651 Публикации | Добавить в корзину |
Родственные гены
Внутриутробная гипоксия исследовалась против:
Связанные пути
Внутриутробная гипоксия связана с:
Связанные болезни
Внутриутробная гипоксия изучалась в отношении таких заболеваний, как:
Связанные PTM
Внутриутробная гипоксия изучалась в отношении посттрансляционных модификаций (ПТМ), включая:
Альтернативные названия
Внутриутробная гипоксия также известна как внутриматочная гипоксия.




 е. возникает быстро и неожиданно
е. возникает быстро и неожиданно